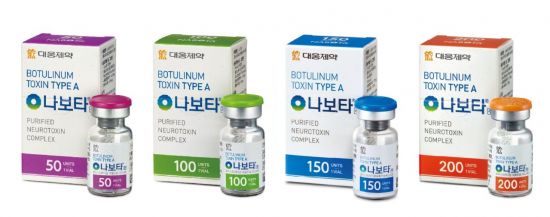
[아시아경제 서소정 기자] 대웅제약의 보툴리눔톡신 '나보타'가 미국 시장 진출 막바지 단계에 돌입했다.
대웅제약은 2일(현지시간) 나보타의 미국 시판허가를 위한 보완자료를 미 식품의약국(FDA)에 제출하고 심사 재개를 신청했다고 3일 밝혔다. 이는 지난 5월 FDA로부터 수령한 최종 보완요구 공문(CRL)에 따른 후속 조치로, FDA는 CRL을 통해 나보타의 생물학적제제 허가신청 서류에 대한 보완을 요구한 바 있다.
심사가 재개되면 최종 결과가 나올 때까지 통상 6개월이 소요되는 것으로 알려져 있다. 나보타의 FDA 시판허가 여부는 내년 상반기에 결정될 전망이다.
서소정 기자 ssj@asiae.co.kr
꼭 봐야할 주요뉴스
 "저 사람 냄새 때문에 괴로워요"…신종 직장내 괴...
마스크영역
"저 사람 냄새 때문에 괴로워요"…신종 직장내 괴...
마스크영역
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>

















![6만7000달러선 횡보…日거래소 해킹 충격[비트코인 지금]](https://cwcontent.asiae.co.kr/asiaresize/269/2023103108282634339_1698708506.png)
![[테크토크]클라우드 느려터져서 택배로 데이터 받아요](https://cwcontent.asiae.co.kr/asiaresize/269/2024053113584191911_1717131521.jpg)

![[뉴욕다이어리]'오바마 향수' 부르는 역대급 비호감 美 대선](https://cwcontent.asiae.co.kr/asiaresize/269/2024060209423794098A.jpg)
![[베이징 다이어리] 美 기업 손 들어준 중국](https://cwcontent.asiae.co.kr/asiaresize/269/2024060216185584810A.jpg)
![[과학을읽다]](https://cwcontent.asiae.co.kr/asiaresize/269/2024060216174273015A.jpg)






![[포토] 일주일 앞으로 다가온 현충일](https://cwcontent.asiae.co.kr/asiaresize/113/2024053109002591299_1717113625.jpg)
![[이미지 다이어리] '예스키즈존도 어린이에겐 울타리'](https://cwcontent.asiae.co.kr/asiaresize/276/2024052917032389151_1716969803.jpg)
![[포토] 시트지로 가린 창문 속 노인의 외침 '지금의 나는 미래의 너다'](https://cwcontent.asiae.co.kr/asiaresize/276/2024052913225588618_1716956574.jpg)



![[뉴스속 용어]심상찮은 '판의 경계'‥아이슬란드서 또 화산 폭발](https://cwcontent.asiae.co.kr/asiaresize/113/2024053015501190632_1717051811.jpg)
![[뉴스속 용어]한-UAE 'CEPA' 체결, FTA와 차이점은?](https://cwcontent.asiae.co.kr/asiaresize/276/2024052915593788994_1716965977.jpg)
![[뉴스속 용어]'거대언어모델(LLM)' 개발에 속도내는 엔씨소프트](https://cwcontent.asiae.co.kr/asiaresize/276/2022032415383891705_1648103918.jpg)
 가장 많이 읽힌 뉴스를 제공합니다. 집계 기준에 따라 최대 3일 전 기사까지 제공될 수 있습니다.
가장 많이 읽힌 뉴스를 제공합니다. 집계 기준에 따라 최대 3일 전 기사까지 제공될 수 있습니다.
![한 벌 1000만원도 입는다…'재벌들의 유니클로'가 뭐길래 [럭셔리월드]](https://cwcontent.asiae.co.kr/asiaresize/269/2024053115494592089_1717138185.jpg)








