"첨단바이오의약품 이상사례 발생시 6개월내 대처방안 보고"
[아시아경제 조현의 기자] 앞으로 바이오 업체는 자사의 유전자치료제 등 첨단바이오의약품이 사용된 후 중대한 이상사례가 발생할 경우 15일 이내에 조사계획을 보고하고 6개월 안에 대처 방안을 보고해야 한다.
식품의약품안전처는 7일 "첨단바이오의약품 사용 후 중대한 이상사례가 발생할 경우 철저히 조사와 함께 사용중단 등 신속한 조치가 이뤄진다"며 이같이 밝혔다.
바이오의약품의 품질과 안전에 대한 관리를 강화하고 신속한 제품화를 지원하기 위해 첨단재생바이오법 하위법령을 제정해 본격적으로 시행한 데 따른 것이다.
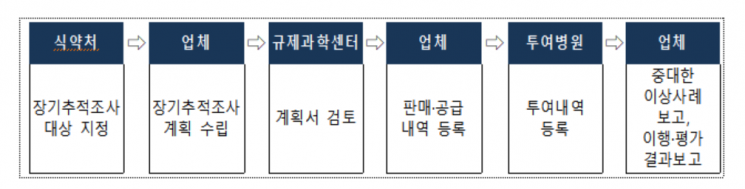
장기추적조사 대상으로 지정된 첨단바이오의약품은 업체가 제품을 판매하기 전까지 장기추적조사계획을 식약처에 제출해야 한다.
장기추적조사 대상 첨단바이오의약품을 투여하는 의사는 환자의 동의를 받아 첨단바이오의약품 규제과학센터에 환자의 인적사항을 등록하고 업체는 장기추적조사의 진행 상황을 식약처에 보고해야 한다.
중대한 이상사례가 발생한 경우 업체는 15일 이내에 식약처에 조사계획을 보고하고 6개월 이내에 발생 원인과 약물과의 인과관계와 대처 방안을 수립해 보고해야 한다.
식약처는 첨단바이오의약품의 원료로 사용하는 인체세포 등을 전문적으로 취급하는 업종을 신설하고 이를 허가하기 위한 절차와 인체세포등의 품질 및 안전성 확보를 위한 세부 기준을 마련했다.
세포처리시설과 인체세포 등 관리업 운영을 위해선 시설·인력·장비 등을 갖춰 허가를 신청해야 하고 서류검토와 실태조사를 거쳐 적합한 경우 승인받게 된다.
인체세포 등 관리업자는 시설·장비에 대한 정기적인 점검과 인체세포등의 품질검사 등을 실시해야 하며 위해인체세포 등을 발견한 경우 식약처에 즉시 보고해야 한다.
현재 시판 중인 세포치료제는 안전성과 품질기준 등에 대해 다시 한 번 검증해 품목허가 할 계획이다.
식약처는 아울러 신속한 개발이 필요한 첨단바이오의약품을 '신속처리 대상'으로 지정하고 개발 초기부터 맞춤형 심사, 우선 심사를 통해 제품화를 지원할 방침이다.
신속처리 대상은 대체치료제가 없는 중대한 질환, 희귀질환관리법에 따른 희귀질환, 대유행 감염병의 예방·치료를 목적으로 하는 첨단바이오의약품이다. 지정된 의약품이 초기 임상시험 결과 또는 임상시험 과정에서 안전성·유효성이 확보됨을 확인할 수 있는 자료를 제시하는 경우 추후 임상시험 자료를 제출하는 것을 조건으로 허가하게 된다.
식약처는 아울러 바이오의약품에 대한 종합적인 정보와 기술을 지원하는 기관으로 '한국의약품안전관리원'을 지정하고 백신 개발을 지원하기 위해 '백신안전기술지원센터'를 설립한다.
꼭 봐야 할 주요 뉴스
 상장 첫날 70% 폭등 "엔비디아 독주 끝나나"…AI ...
상장 첫날 70% 폭등 "엔비디아 독주 끝나나"…AI ...
이의경 처장은 "안전과 품질이 확보된 바이오의약품의 제품화 지원을 위해 맞춤형 허가 정책을 운영해 나가겠다"며 "첨단재생바이오법의 시행으로 첨단바이오의약품의 품질 및 안전관리를 강화해 제품 경쟁력을 높이는 한편 희귀·난치질환자에게 새로운 치료 기회를 제공하게 될 것으로 기대한다"고 밝혔다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>







![[폴폴뉴스]지선 앞두고 결집한 野…野 지선 승리해야 33%, 3%p↑](https://cwcontent.asiae.co.kr/asiaresize/308/2026051510373164594_1778809051.jpg)







![[Why&Next]해외매출 비중 90%…K-뷰티, 수익성 엇갈린 '이 공식'](https://cwcontent.asiae.co.kr/asiaresize/308/2026051116551658156_1778486116.png)

![[시시비비] 과학, 맹신, 사기… 혼돈의 딥테크 주식](https://cwcontent.asiae.co.kr/asiaresize/308/2026051407271078513A.jpg)
![[초동시각]코스피8000 시대, AI투자도 대전환 시급](https://cwcontent.asiae.co.kr/asiaresize/308/2026051409011380770A.jpg)
![[기자수첩]'현대판 러다이트' 멈춰선 공장의 의미](https://cwcontent.asiae.co.kr/asiaresize/308/2026051510403924523A.jpg)










![[미중 정상회담]테이블에 무역휴전 연장…"45兆 상품관세 인하 논의"](https://cwcontent.asiae.co.kr/asiaresize/309/2026051411260162853_1778725560.jpg)
![[미중 정상회담]트럼프 "상호주의 더욱 발전"…시진핑 "공동이익, 분란 이겨"](https://cwcontent.asiae.co.kr/asiaresize/309/2026051411462362902_1778726783.jpg)







