UNIST 연구팀, 노화세포 선택적 제거 기술 개발
노화 세포를 선택적으로 제거할 수 있는 기술이 개발돼 노인성 질환 치료의 새로운 비전을 제시할 수 있을 것으로 기대된다.
UNIST 화학과 유자형 교수팀과 건국대학교 정혜원 교수팀은 노화 세포의 미토콘드리아 안에 인공단백질을 형성해 노화 세포를 선택적으로 제거하는 기술을 개발했다.
개발된 기술은 노화 세포막에 과발현된 수용체를 선택적으로 표적할 수 있으며 정상세포에 비해 높게 발현된 활성산소를 매개로 인공단백질 구조체도 형성할 수 있어 정상세포에 악영향 없이 노화 세포만 선택적으로 제거할 수 있게 됐다.
인간이 노화함에 따라 정상세포는 암세포로 변할 가능성이 커져 세포는 암세포로의 발전을 막기 위해 자발적으로 노화 세포로 변한다. 하지만 노화 세포의 축적은 각종 염증을 유발하고 노인성 질환의 원인이 된다.
연구팀은 노인성 질환을 치료를 위해 노화 세포를 표적할 수 있는 방법을 연구했다.
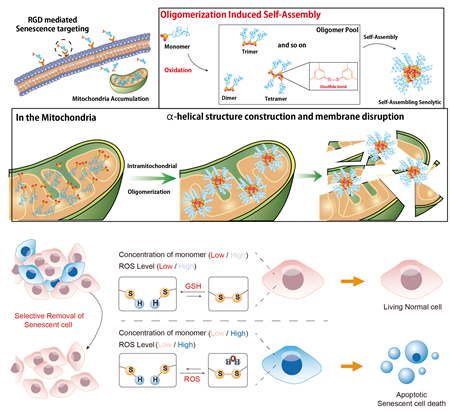
탄소를 기반으로 한 ‘유기 분자’는 이황화 결합을 할 수 있는 부분과 노화 세포를 표적할 수 있는 부분으로 구성된다. 이황화 결합은 황 분자끼리 산화 과정을 거쳐 결합되는 형태인데 활성산소와 같은 물질로 산화를 촉진시킬 수 있다.
활성산소는 산소를 사용하는 과정에서 생성되는 부산물로 노화 세포 안의 미토콘드리아는 이런 활성산소가 과발현된다. 과발현된 활성산소는 이황화 결합을 촉진시키게 되고 분자끼리 결합하는 소중합체(올리고머)를 형성한다.
연구팀은 올리고머의 자기조립으로 나선형 구조를 띠는 ‘알파 헬릭스’가 표면에 생기는 인공단백질을 만드는 기술을 개발했다. 이러한 구조체는 미토콘드리아 막에 강하게 결합해 막을 파괴하며 세포의 자가사멸을 유도하게 된다.
연구팀은 개발된 기술을 노인성 건성황반변성을 가진 쥐 모델에 적용해 노화 세포가 효율적으로 제거되고 망막조직의 기능이 정상 범위로 돌아오는 것을 확인했다. 또 자연 노화된 쥐 모델의 망막조직에서도 노화 세포가 선택적으로 제거되는 것을 확인했다.
화학과 유자형 교수는 “노화 세포의 미토콘드리아 표적으로 기능장애를 유도해 노화 세포가 선택적으로 제거됨을 실제 실험 쥐에서 확인했다”며 “이와 같은 접근법은 기존 노화 치료제와는 다른 접근법으로 노인성 질병 치료에 새로운 패러다임을 제시할 것이다”고 설명했다.
공동연구자 퓨전바이오텍 김채규 대표는 “세포 내 소기관을 표적해 독성 문제를 최소화하고 넓은 치료용량 범위(therapeutic window)를 확보할 수 있다”며 “향후 전임상과 임상시험 설계 시 유리한 조건을 가질 수 있을 것”으로 기대했다.
꼭 봐야 할 주요 뉴스
![100조 날리게 생겼는데…"삼성 파업은 역대급 특수" 가격 20% 폭등하고 난리 [대만칩통신]](https://cwcontent.asiae.co.kr/asiaresize/93/2026051416263163580_1778743590.jpg) 100조 날리게 생겼는데…"삼성 파업은 역대급 특수...
100조 날리게 생겼는데…"삼성 파업은 역대급 특수...
이번 연구 결과는 과학기술정보통신부 한국연구재단의 중견 연구와 바이오·의료기술개발사업의 지원으로 이뤄졌으며 화학 저널로 저명한 미국화학학회지 Journal of the American Chemical Society에 9월 4일 자로 온라인 게재됐다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>


![[초동시각]애물단지가 된 필리버스터](https://cwcontent.asiae.co.kr/asiaresize/308/2026051513484496581A.jpg)
![[기자수첩]'현대판 러다이트' 멈춰선 공장의 의미](https://cwcontent.asiae.co.kr/asiaresize/308/2026051513493797137A.jpg)
![[남산길 산책]2026년 아비뇽, 세계에 선보일 K-연극](https://cwcontent.asiae.co.kr/asiaresize/308/2026051513455791682A.jpg)
!["편의점 10곳 돌아도 못 샀다" 난리…벌써 1억개 팔린 빵 정체[지금 사는 방식]](https://cwcontent.asiae.co.kr/asiaresize/308/2026051314412961326_1778650889.jpg)












![AI 때문에 일자리 사라진다더니…구인 800% 폭증한 '이 직종' [테크토크]](https://cwcontent.asiae.co.kr/asiaresize/308/2026051413392963075_1778733569.jpg)





!["집 지어지면 먼저 연락 주세요" 자산가들 '눈독'…200억원 초고가주택 들어서나[부동산AtoZ]](https://cwcontent.asiae.co.kr/asiaresize/309/2026051609430065520_1778892181.jpg)

![100조 날리게 생겼는데…"삼성 파업은 역대급 특수" 가격 20% 폭등하고 난리 [대만칩통신]](https://cwcontent.asiae.co.kr/asiaresize/309/2026051416263163580_1778743590.jpg)

![[타보니]"최상위, 그 너머에"…메르세데스-마이바흐 GLS 600'](https://cwcontent.asiae.co.kr/asiaresize/309/2026051509582364441_1778806703.jpg)


!["HBM도 넘본다"…삼성·SK, 中 추격에도 '초격차' 유지하려면[칩톡]](https://cwcontent.asiae.co.kr/asiaresize/309/2025021710490034501_1739756940.jpg)








