식약처, 코로나19 진단키트 첫 정식허가
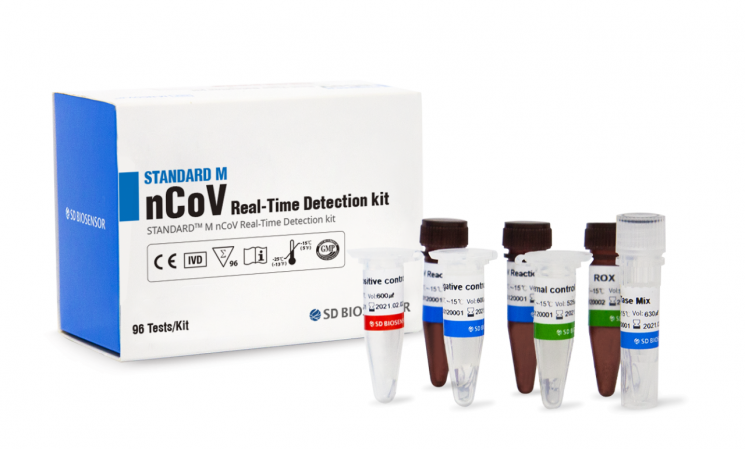
[아시아경제 최대열 기자] 에스디바이오센서가 만든 신종 코로나바이러스감염증(코로나19) 진단시약이 정식 허가를 받았다고 식품의약품안전처가 1일 밝혔다. 그간 긴급사용승인에 따라 일선 현장에서는 다수 제품을 써왔는데 정식으로 허가를 받은 건 이번이 처음이다.
이 품목은 분자진단(RT-PCR)방식으로 이미 긴급사용승인과 수출용 허가는 받은 상태다. 이번 허가는 임상시험과 품질검사기준(GMP) 등 체외진단의료기기법에 따른 절차를 거쳐 국내 제조허가를 받은 것이다.
통상 정식 허가는 1년 이상 걸리지만 이번에는 4개월여 만에 절차를 마쳤다. 식약처가 코로나19 유행에 대비, 지난 4월 진단시약에 대한 신속허가 지원방안을 마련했기에 가능했다. 신속허가 지원방안은 코로나19 진단키트의 국내 제조허가 획득을 독려하기 위한 것으로 올해 10월까지 한시적으로 운영한다.
꼭 봐야 할 주요 뉴스
 상장 첫날 70% 폭등 "엔비디아 독주 끝나나"…AI ...
상장 첫날 70% 폭등 "엔비디아 독주 끝나나"…AI ...
AD
양진영 식약처 차장은 "이번 제품은 감염병 위기 상황에 한시적으로 사용되는 긴급사용승인 제품 가운데 처음으로 임상시험, 품질검사기준 등 심사평가를 거쳐 국내 허가를 받았다"면서 "품질에 대한 국제 신뢰도를 높이고 국내 의료현장에서 코로나19 진단시약을 안정적으로 공급할 수 있는 길이 열렸다는 점에서 의미가 있다"고 말했다.
최대열 기자 dychoi@asiae.co.kr
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>

![이동훈 "당장 투표하면 11:5, 정원오 굉장한 위기"[시사쇼]](https://cwcontent.asiae.co.kr/asiaresize/308/2026051514493165024_1778824170.jpg)

![[르포]"與 독주 안돼" "젊은 사람은 달라"…반반 갈린 창원 민심](https://cwcontent.asiae.co.kr/asiaresize/308/2026051507270263925_1778804565.jpg)








![[초동시각]애물단지가 된 필리버스터](https://cwcontent.asiae.co.kr/asiaresize/308/2026051513484496581A.jpg)
![[기자수첩]'현대판 러다이트' 멈춰선 공장의 의미](https://cwcontent.asiae.co.kr/asiaresize/308/2026051513493797137A.jpg)
![[남산길 산책]2026년 아비뇽, 세계에 선보일 K-연극](https://cwcontent.asiae.co.kr/asiaresize/308/2026051513455791682A.jpg)

























