식약처 "국내 유통 '잔탁'서 발암 우려 물질 검출 안 돼"
-식약처, 잔탁 등 라니티딘 제제 발암 우려 물질(NDMA) 안전성 조사 실시
-원료의약품 제조소 전체로 조사 대상 확대
[아시아경제 박혜정 기자] 식품의약품안전처는 위궤양 치료제 '잔탁' 등 일부 라니티딘 계열의 제산제에서 '발암 우려 물질'로 분류된 불순물이 검출되지 않았다고 16일 밝혔다. 지난 14일 N-니트로소디메틸아민(NDMA)이 잔탁 등 라니티딘 계열의 일부 약에서 소량 검출됐다는 미국 식품의약국(FDA)과 유럽의약품청(EMA)의 발표 이후 국내 유통 중인 잔탁과 잔탁에 사용하는 원료제조소에서 생산된 라니티딘을 검사한 결과다.
NDMA는 세계보건기구 국제암연구소(IARC)가 인간에게 발암물질로 작용할 가능성 있는 물질(2A)로 분류했으며 지난해 발사르탄 계열의 고혈압약에서 검출됐었다.
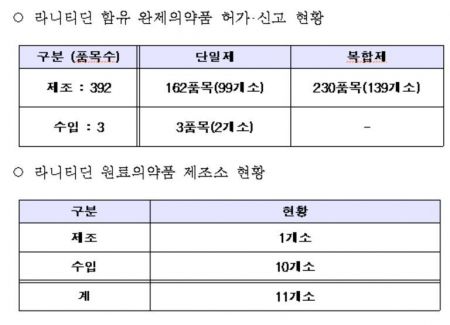
이번에 식약처가 검사한 제품은 한국 GSK가 허가받은 잔탁정 75㎎(일반의약품)·잔탁정 150㎎(전문의약품)·잔탁주 2㎖(주사제) 등 잔탁 3개 품목 29개 제품(제조번호)과 잔탁에 사용된 원료 라니티딘 6개 등 총 35개다.
식약처는 현재 수입 또는 국내 제조되는 모든 라니티딘 원료(제조소 11개)와 이를 사용한 의약품 395개 품목을 대상으로 수거·검사를 확대할 계획이다.
라니티딘은 위산 과다, 속쓰림, 위·십이지장궤양, 역류성식도염 등에 사용하는 의약품이다. 라니티딘 제제에서 NDMA가 검출된 원인은 조사 중이다. 현재 식약처를 포함한 미국, 유럽 각국 규제기관들은 발사르탄 경우과 다른 것으로 추정하고 있다. FDA와 EMA 캐나다 의약품청에서는 환자들에게 일부 라니티딘 제제에서 검출된 NDMA의 양이 아주 소량인 만큼 복용 중단을 권고하지 않고 있다. 처방을 변경하려면 전문가와 상담하고 일반의약품의 경우 동일 효능의 다른 제품을 사용할 수 있다고 설명하고 있다.
꼭 봐야 할 주요 뉴스
 "세계 1등하겠다"더니 급브레이크…"정부 믿고 수...
"세계 1등하겠다"더니 급브레이크…"정부 믿고 수...
식약처 관계자는 "이번에 수거한 1개 제조소 외에 10개 제조소에서 생산돼 유통 중인 원료의약품에 대해 수거·검사를 실시하고 그 결과에 따라 완제의약품에 대해서도 단계적으로 검사할 것"이라며 "현재까지 검사 결과 NDMA가 검출되지 않고 있는 만큼 회수 등의 조치는 하지 않고 있다"고 말했다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>


![[시시비비] 과학, 맹신, 사기… 혼돈의 딥테크 주식](https://cwcontent.asiae.co.kr/asiaresize/308/2026051407271078513A.jpg)
![[초동시각]코스피8000 시대, AI투자도 대전환 시급](https://cwcontent.asiae.co.kr/asiaresize/308/2026051409011380770A.jpg)
![[기자수첩]소상공인에겐 너무 먼 일·가정 양립](https://cwcontent.asiae.co.kr/asiaresize/308/2026051409481693494A.jpg)









![[Why&Next]해외매출 비중 90%…K-뷰티, 수익성 엇갈린 '이 공식'](https://cwcontent.asiae.co.kr/asiaresize/308/2026051116551658156_1778486116.png)
















![[미중 정상회담]테이블에 무역휴전 연장…"45兆 상품관세 인하 논의"](https://cwcontent.asiae.co.kr/asiaresize/309/2026051411260162853_1778725560.jpg)
![[미중 정상회담]트럼프 "상호주의 더욱 발전"…시진핑 "공동이익, 분란 이겨"](https://cwcontent.asiae.co.kr/asiaresize/309/2026051411462362902_1778726783.jpg)