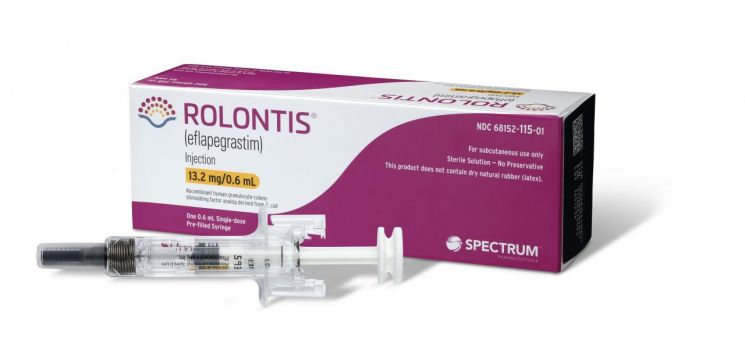
한미 '롤론티스', FDA 허가 절차 본격 돌입
[아시아경제 이춘희 기자] 한미약품 한미약품 close 증권정보 128940 KOSPI 현재가 446,500 전일대비 1,500 등락률 +0.34% 거래량 66,241 전일가 445,000 2026.05.14 13:14 기준 관련기사 한미약품, '혁신성장부문' 신설…4개 부문 통합 체제로 재편 북경한미, 창립 첫 4000억 매출 달성…배당 누적 1380억 그룹 환원 한미약품, R&D 비중 16.6%…매출·순이익 증가 속 투자 확대 의 파트너사 스펙트럼이 미국 식품의약국(FDA)에 재신청한 호중구감소증 치료제 ‘롤론티스’의 시판허가(BLA) 심사가 본격 시작됐다.
스펙트럼은 11일(현지시간) FDA가 롤론티스의 BLA를 승인하고 시판 허가를 위한 공식 심사 절차에 들어갔다고 밝혔다. 스펙트럼은 당초 지난해 8월 FDA에 허가 신청을 냈지만 제조시설 관련 보완을 요구받고 지난달 18일 허가를 재신청했다.
이에 따라 '처방의약품 신청자 수수료 법(PDUFA)'에 따라 FDA는 오는 9월9일 이전에 최종 허가 여부를 결정할 예정이다. 이 기간 내에 롤론티스 원료를 생산하는 한미약품 평택 바이오플랜트에 대한 FDA의 실사도 진행될 예정이다.
꼭 봐야 할 주요 뉴스
 텀블러에 담아 입 대고 마셨는데…24시간 지난 후...
텀블러에 담아 입 대고 마셨는데…24시간 지난 후...
톰 리가 스펙트럼 사장은 ““FDA의 롤론티스 BLA 신청 승인은 중요한 진전"이라며 "FDA 심사 절차에 적극적으로 협력하고 있으며 롤론티스의 최종 승인을 기대하고 있다"고 말했다. 권세창 한미약품 대표이사 사장도 “롤론티스의 FDA 허가를 위한 마지막 관문에 공식적으로 진입했다”며 “롤론티스의 성공적인 시판 승인을 위해 파트너사인 스펙트럼과 긴밀히 협력해 나가겠다”고 말했다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>












![[단독]문신사법 시행 앞두고 엇갈린 법원…‘눈썹문신 무죄’ 대법 심리 착수](https://cwcontent.asiae.co.kr/asiaresize/308/2020013114494834033_1580449788.jpg)




![[시시비비] 과학, 맹신, 사기… 혼돈의 딥테크 주식](https://cwcontent.asiae.co.kr/asiaresize/308/2026051407271078513A.jpg)
![[초동시각]코스피8000 시대, AI투자도 대전환 시급](https://cwcontent.asiae.co.kr/asiaresize/308/2026051409011380770A.jpg)
![[기자수첩]소상공인에겐 너무 먼 일·가정 양립](https://cwcontent.asiae.co.kr/asiaresize/308/2026051409481693494A.jpg)








!["10년 만에 해냈다…이번엔 진짜" 반도체 호황에 1분기 경상흑자 '사상최대'[BOK포커스]](https://cwcontent.asiae.co.kr/asiaresize/309/2026051315410261534_1778654463.png)