GIST, 세포 속 청소 돕는 단백질 복합체 구조 규명
자가포식 관련 질환 연구 새 지평 기대
[아시아경제 호남취재본부 윤자민 기자] GIST(총장 김기선)는 세포 로지스틱스 연구센터(센터장 전영수) 전영수 교수(생명과학부)와 UNIST 이창욱 교수(생명과학부) 공동 연구팀이 ‘자가포식이 단백질의 4차 구조(protein quaternary structure)를 통해 선택적으로 조절된다’는 사실을 규명했다고 16일 밝혔다.
공동연구팀은 어떤 물질을 분해할지 선택하고 리소좀(lysosome)으로 옮기는 데 단백질 복합체의 구조가 큰 역할을 하고 있다는 사실을 밝혀냈다.
이는 향후 자가포식 관련 질환 연구에 새로운 방향을 제시할 것으로 기대된다.
세포 속에 노폐물이 쌓이거나 바이러스 같은 외부 침입자가 들어오면 ‘자가포식(autophagy)’이 시작되는데 이는 불필요한 물질을 세포 내에서 스스로 분해하는 일종의 ‘청소’다.
이 작용은 리소좀이라는 공간에서 일어나는데 여기로 가져올 물질을 선택하는 원리가 밝혀진 것이다.
세포 내 불필요한 물질을 골라내 리소좀까지 옮기는 데는 다양한 단백질이 관여한다.
대표적으로 ‘Vac8(Vacuole related 8) 단백질’이 잘 알려져 있는데 이 단백질이 어떤 단백질과 결합하느냐에 따라 자가포식 유형이 결정된다.
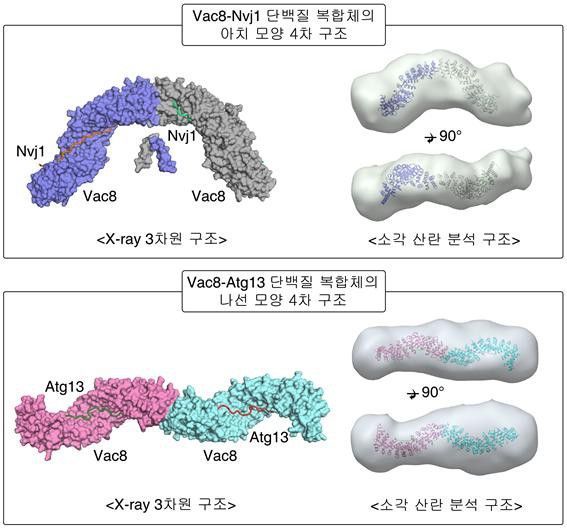
Vac8 단백질이 Nvj1(Nucleus-vacuole junction 1) 단백질과 결합하면 세포핵 일부분을 분해하는 자가포식(PMN)이 작동하는 반면, Atg13(Autophagy Related 13) 단백질과 결합하면 세포질 가수분해 효소를 리소좀으로 수송하는 ‘Cvt 경로(Cytoplasm-to-vacuole targeting pathway)’를 작동시킨다. 하지만 Vac8가 단백질이 이들 단백질과 결합하는 구체적인 원리는 밝혀지지 않았다.
이번 연구에서는 단백질 결정을 이용한 ‘X-선 결정법’과 ‘X-선 소각 산란 분석법’을 이용해 Vac8 단백질이 결합하는 단백질에 따라 4차 구조가 달라진다는 사실을 밝혀냈다.
달라진 구조에 따라 자가포식의 유형도 결정됐다.
연구팀은 효모를 이용해 Atg13 단백질 결합에 관여하는 아미노산 돌연변이를 유도해 검증도 진행했다. 실험 결과 Atg13 결합 구조에 문제가 생기자 PMN 자가포식은 나타났지만 Cvt 관련 반응은 나타나지 않았다. 단백질 4차 구조에 이상이 나타나면 특정 자가포식이 일어나지 않음을 입증한 것이다.
GIST 전영수 교수는 “이번 연구는 하나의 단백질이 어떻게 다양한 형태의 자가포식 과정을 선택적으로 매개할 수 있는지를 규명한 연구성과다”며 “단백질 4차 구조를 이용해 파킨슨병이나 치매, 암, 노화 등 자가포식 관련 질환의 치료법을 찾는 연구에 새로운 방향을 제시할 것으로 기대한다”고 말했다.
꼭 봐야 할 주요 뉴스
 삼성 주춤하자 무섭게 치고 올라왔다…1년 만에 흑...
삼성 주춤하자 무섭게 치고 올라왔다…1년 만에 흑...
한편 이번 연구는 한국연구재단이 지원하는 선도연구센터지원사업(SRC·세포 로지스틱스 연구센터) 및 GIST 연구원(GRI)의 지원을 받아 수행됐다. 연구 성과는 자가포식 연구분야 최고 권위 학술지인 ‘오토파지(Autophagy, IF=11.1)’ 저널에 지난 12일 자 온라인으로 게재됐다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>


![2주만 참으면 항공권 '핫딜' 뜬다…해외여행 들썩[비주얼뉴스]](https://cwcontent.asiae.co.kr/asiaresize/308/2026051815013167296_1779084091.jpg)


![[르포]"전가구 100% 남향·한강조망"…DL이앤씨, 압구정5구역 조합원 표심잡기](https://cwcontent.asiae.co.kr/asiaresize/308/2026051812040467045_1779073444.jpg)
!['마이쭈'보다 싼 주사제…소아 필수약인데 만들수록 손해[Why&Next]](https://cwcontent.asiae.co.kr/asiaresize/308/2026051811210766990_1779070866.png)
![[단독]예산보호막 사라진 디지털배움터, 재정열악 지자체선 축소·소멸될 수도](https://cwcontent.asiae.co.kr/asiaresize/308/2026051808275866381_1779060477.png)
![[초동시각]증시활황이 불러온 긍정 효과들](https://cwcontent.asiae.co.kr/asiaresize/308/2026051811030357256A.jpg)
![[에너지토피아]전기 버리는 유럽, 남의 일 아니다](https://cwcontent.asiae.co.kr/asiaresize/308/2026051815313149170A.jpg)
![[트레이드 오프]안보보다 경제가 급했다](https://cwcontent.asiae.co.kr/asiaresize/308/2026051811180517690A.jpg)













![[속보]법원, 삼성전자 노조에 제동…파업 범위 위반 시 ‘하루 1억’ 배상](https://cwcontent.asiae.co.kr/asiaresize/309/2026051719315966137_1779013920.png)




![유통책이 물었다…유흥가, 얼마나 알고 있나[취藥국가]①](https://cwcontent.asiae.co.kr/asiaresize/309/2026051318172661825_1778663847.png)
![[취藥국가]⑤"감옥에서 김치까지"…캄보디아 총책 '송'](https://cwcontent.asiae.co.kr/asiaresize/309/2026012809163418359_1769559394.jpg)