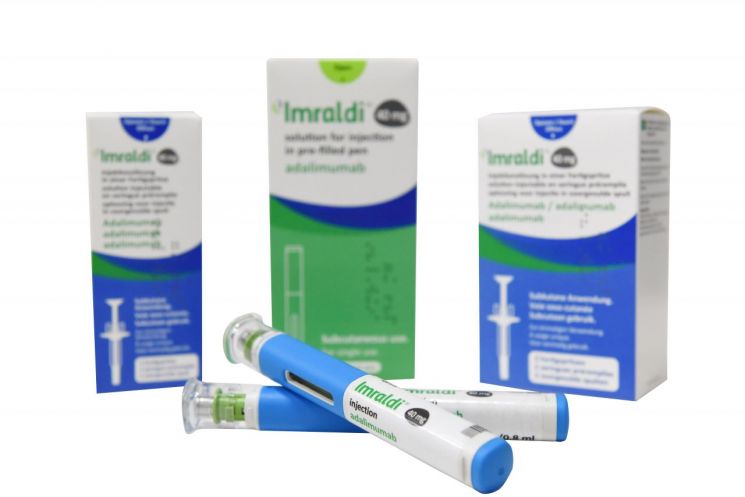
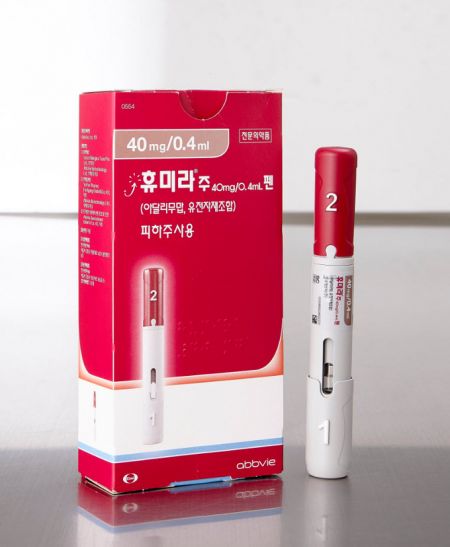
삼성바이오에피스, '휴미라' 바이오시밀러 리얼월드 관찰 데이터 공개
휴미라 바이오시밀러 'SB5'
伊 밀라노 EADV 학술대회에서 발표
2018년 유럽 출시 후 실제 처방 환자 데이터
72%가 3년 넘게 SB5 처방 유지해
내년 미국 시장 진출 앞두고 각축전
[아시아경제 이춘희 기자] 28조원에 달하는 애브비의 자가면역질환 치료제 '휴미라(성분명 아달리무맙)' 바이오시밀러 개발 경쟁이 계속 치열해지고 있다. 내년 문호가 개방되는 미국 시장 진출을 앞두고 리얼월드 데이터(RWD)를 공개하는 등 효과성과 안전성 등을 입증하는 싸움이 벌어지고 있다.
삼성바이오에피스는 휴미라 바이오시밀러로 개발 중인 'SB5'의 3년 추적 관찰 데이터를 유럽 피부과학회 학술대회(EADV Congress)에서 발표한다고 7일 밝혔다. 올해로 31회를 맞는 EADV는 유럽의 저명한 피부과학회다. 7~10일 나흘간 이탈리아 밀라노 현지와 온라인으로 동시에 진행된다.
삼성바이오에피스는 이번에 영국 지역 환자 등록부(레지스트리) '영국 피부과 생물학자협회 및 면역측정기 협회 레지스트리(BADBIR) 스터디에서 관찰된 중등도~중증(Moderate-to-Severe) 건선 환자를 대상으로 한 SB5 처방 후 3년간의 추적 연구 결과'의 초록을 공개할 예정이다. BADBIR는 건선에 대한 생물학적 치료제의 장기 안전성을 평가하는 영국 및 아일랜드의 레지스트리다. 삼성바이오에피스는 2016년 5월부터 연구에 참여해왔다.
초록에 따르면 추적 관찰 연구는 2019년 6월부터 지난해 8월까지 BADBIR에 등록된 SB5를 처방받은 건선 환자 1059명을 대상으로 이뤄졌다. 그 결과 환자들이 3년간 치료를 지속하는 비율은 72.1%로 나타났다. 1년차, 2년차, 3년차 누적 지속률은 각각 79.7%, 73.5%, 72.1%였다.
정진아 삼성바이오에피스 메디컬 어페어스(Medical Affairs) 그룹장은 “건선에 처방되는 아달리무맙 바이오시밀러의 효능과 안전성을 나타내는 장기간의 RWD가 흔치 않은 가운데, 이번 연구 결과를 통해 SB5가 오리지널 의약품 수준의 안전성과 효능을 보유했음을 입증했다”고 전했다.
애브비가 개발한 휴미라는 류마티스 관절염, 크론병, 판상 건선 등의 면역 매개 질환 치료제다. 2020년까지 9년 연속 세계 매출 1위를 기록한 블록버스터 의약품이다. 지난해에는 매출 207억달러(약 28조7109억원)로, 매출 368억달러(약 51조원)를 올린 화이자 코로나19 백신 ‘코미나티’에 왕좌를 빼앗겼지만 내년에는 다시 1위로 올라설 가능성이 제기된다.
이미 한국·유럽 등에서는 SB5가 제품명 '임랄디'로 이미 2018년부터 시판되는 등 바이오시밀러 경쟁이 본격화됐지만 미국 시장은 여전히 휴미라가 독점하고 있다. 물질특허가 2016년 만료됐지만 애브비가 특허 분쟁을 통해 출시를 지연시키면서 대부분 내년 출시로 합의가 이뤄졌다. FDA 기준 ▲암제비타(암젠) ▲실테조(베링거인겔하임) ▲하이리모즈(산도스) ▲하드리마(SB5의 미국 출시명) ▲아브릴라다(화이자) ▲훌리오(비아트리스) ▲유심리(코헤루스) 등 7개 품목이 승인됐고 이들 모두 내년 중 출시를 준비하고 있다. 셀트리온 셀트리온 close 증권정보 068270 KOSPI 현재가 195,100 전일대비 4,600 등락률 +2.41% 거래량 701,802 전일가 190,500 2026.05.14 15:30 기준 관련기사 셀트리온 유럽 램시마 합산 점유율 70%…신·구 제품군 성장세 지속 셀트리온, 다우존스 지속가능경영 월드 지수 2년 연속 편입 셀트리온, 프랑스 헬스케어 기업 지프레 인수…"약국 영업망 확보" 도 '유플라이마(CT-P17)'의 내년 7월 출시를 목표로 승인 절차를 진행하고 있다.
삼성바이오에피스는 최근 미국 식품의약국(FDA)에서 하드리마의 고농도 제형(HCF, 100㎎/㎖) 허가를 받는 등 미국 시장 출시를 위한 준비를 서두르고 있다. 기존 저농도 제형(50㎎/㎖)보다 약물 투여량이 적어 환자의 선호도가 높다.
꼭 봐야 할 주요 뉴스
 텀블러에 담아 입 대고 마셨는데…24시간 지난 후...
텀블러에 담아 입 대고 마셨는데…24시간 지난 후...
고농도 제형에 대한 FDA 허가는 오리지널 의약품인 휴미라를 제외하고는 하드리마가 바이오시밀러 중에서는 최초로 알려졌다. 내년 문이 열리는 미국 시장 선점의 교두보를 마련한 셈이다. 이에 다른 바이오시밀러 개발사들도 HCF 제형 개발에 나서고 있다. 하이리모즈를 개발한 노바티스의 자회사 산도스는 지난 7월 FDA에 HCF 허가를 신청했고, 암제비타를 개발한 암젠 등도 HCF 개발을 진행하고 있다. 셀트리온은 처음부터 유플라이마의 기본 제형을 HCF로 개발했다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>



![[단독]문신사법 시행 앞두고 엇갈린 법원…‘눈썹문신 무죄’ 대법 심리 착수](https://cwcontent.asiae.co.kr/asiaresize/308/2020013114494834033_1580449788.jpg)








![[시시비비] 과학, 맹신, 사기… 혼돈의 딥테크 주식](https://cwcontent.asiae.co.kr/asiaresize/308/2026051407271078513A.jpg)
![[초동시각]코스피8000 시대, AI투자도 대전환 시급](https://cwcontent.asiae.co.kr/asiaresize/308/2026051409011380770A.jpg)
![[기자수첩]소상공인에겐 너무 먼 일·가정 양립](https://cwcontent.asiae.co.kr/asiaresize/308/2026051409481693494A.jpg)










!["10년 만에 해냈다…이번엔 진짜" 반도체 호황에 1분기 경상흑자 '사상최대'[BOK포커스]](https://cwcontent.asiae.co.kr/asiaresize/309/2026051315410261534_1778654463.png)





![[미중 정상회담]테이블에 무역휴전 연장…"45兆 상품관세 인하 논의"](https://cwcontent.asiae.co.kr/asiaresize/309/2026051411260162853_1778725560.jpg)
![[미중 정상회담]트럼프 "상호주의 더욱 발전"…시진핑 "공동이익, 분란 이겨"](https://cwcontent.asiae.co.kr/asiaresize/309/2026051411462362902_1778726783.jpg)