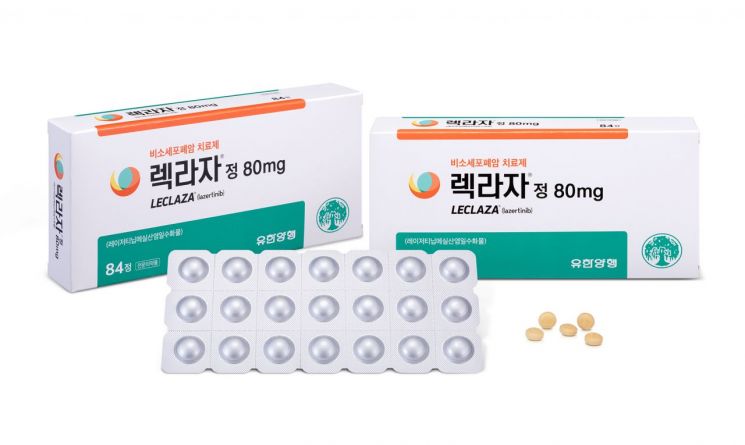
유한 항암 신약 '렉라자' 1차 치료 옵션 위한 임상 3상 성공
13개국 다국가 임상 3상 'LASER301'
대조군 대비 암 진행·사망 위험 55%↓
내년 1Q 적응증 확대 위한 허가 변경 예정
유한양행의 비소세포폐암 치료 신약 ‘렉라자(성분명 레이저티닙)’가 1차 치료제로 사용하기 위한 임상 3상에 성공했다. 현재는 이미 다른 치료를 받은 적이 있는 환자만 렉라자를 사용할 수 있지만 앞으로는 처음부터 렉라자 투여를 통한 치료가 가능해질 것으로 전망된다.
14일 유한양행은 비소세포폐암 환자들에 대한 1차 치료로서 렉라자의 유효성과 안전성을 평가하는 다국가 임상 3상(LASER301) 톱 라인 결과, 1차 유효성 지표를 충족했다고 밝혔다. 이번 임상은 한국, 호주, 터키, 헝가리 등 13개국 119개 국내외 기관에서 환자 393명을 대상으로 진행됐다.
대조군으로 설정한 아스트라제네카의 ‘이레사정(성분명 게피티니브)’ 투약군 대비 렉라자 투여군에서 무진행 생존 기간(PFS)을 분석한 결과, 암의 진행 혹은 이로 인한 사망 위험은 55% 줄어든 것으로 나타났다. 무진행 생존 기간은 항암제의 효능을 평가하는 변수로, 질병이 진행되지 않거나 사망에 이르지 않는 기간이다. 유한양행은 이외에도 객관적 반응률(ORR), 전체 생존 기간(OS) 등 2차 유효성 지표 등을 포함한 상세한 내용을 오는 12월 전문 학회에서 발표할 예정이다.
LASER301을 이끈 조병철 세브란스병원 교수는 “이번 다국가 임상 3상을 통해 레이저티닙이 1차 치료제로서 1차 평가목적을 달성하게 돼 매우 고무적”이라며 “레이저티닙이 전 세계 활성 상피세포 성장인자 수용체(EGFR) 돌연변이 양성 비소세포폐암 환자들에게 새로운 1차 치료 옵션이 될 수 있을 것”이라고 전했다.
렉라자는 EGFR 돌연변이에 선택적으로 작용하는 경구형 3세대 EGFR 티로신 인산화효소 억제제(TKI) 계열 약제다. 이전에 EGFR-TKI로 치료받은 적이 있는 EGFR T790M 변이 양성 국소 진행성 또는 전이성 비소세포폐암 환자를 치료할 목적으로 지난해 1월 식품의약품안전처 품목 허가를 받으면서 31호 국산 신약이 됐고, 이미 국내 누적 매출이 100억원을 넘어서는 등 상업적 성공을 거두고 있다.
다만 지금까지는 다른 치료법으로 1차 치료를 받은 적이 있는 환자를 대상으로 한 2차 치료법으로만 쓰여 왔다. 이번 임상 3상은 1차 치료법으로 렉라자 단독 투여가 가능한지 확인하기 위해 이뤄졌다.
꼭 봐야 할 주요 뉴스
 텀블러에 담아 입 대고 마셨는데…24시간 지난 후...
텀블러에 담아 입 대고 마셨는데…24시간 지난 후...
유한양행 관계자는 "이번 글로벌 임상 3상의 톱 라인 결과 분석을 통해 1차 치료제로서 렉라자의 유효성이 확인됐다"며 "내년 1분기 안으로 국내 적응증 확대를 위한 허가 변경을 신청할 예정"이라고 말했다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>


![[시시비비] 과학, 맹신, 사기… 혼돈의 딥테크 주식](https://cwcontent.asiae.co.kr/asiaresize/308/2026051407271078513A.jpg)
![[초동시각]코스피8000 시대, AI투자도 대전환 시급](https://cwcontent.asiae.co.kr/asiaresize/308/2026051409011380770A.jpg)
![[기자수첩]소상공인에겐 너무 먼 일·가정 양립](https://cwcontent.asiae.co.kr/asiaresize/308/2026051409481693494A.jpg)








![[단독]문신사법 시행 앞두고 엇갈린 법원…‘눈썹문신 무죄’ 대법 심리 착수](https://cwcontent.asiae.co.kr/asiaresize/308/2020013114494834033_1580449788.jpg)












!["10년 만에 해냈다…이번엔 진짜" 반도체 호황에 1분기 경상흑자 '사상최대'[BOK포커스]](https://cwcontent.asiae.co.kr/asiaresize/309/2026051315410261534_1778654463.png)



![[미중 정상회담]테이블에 무역휴전 연장…"45兆 상품관세 인하 논의"](https://cwcontent.asiae.co.kr/asiaresize/309/2026051411260162853_1778725560.jpg)

![[미중 정상회담]트럼프 "상호주의 더욱 발전"…시진핑 "공동이익, 분란 이겨"](https://cwcontent.asiae.co.kr/asiaresize/309/2026051411462362902_1778726783.jpg)