"무허가 원료 사용" 한스바이오메드 인공유방 판매중지
[아시아경제 조현의 기자] 식품의약품안전처는 13일 의료기기 업체 한스바이오메드가 실리콘 겔 인공유방 '벨라젤'을 허가사항과 다른 원료를 사용해 제조한 후 약 7만여 개를 유통한 사실을 확인했다.
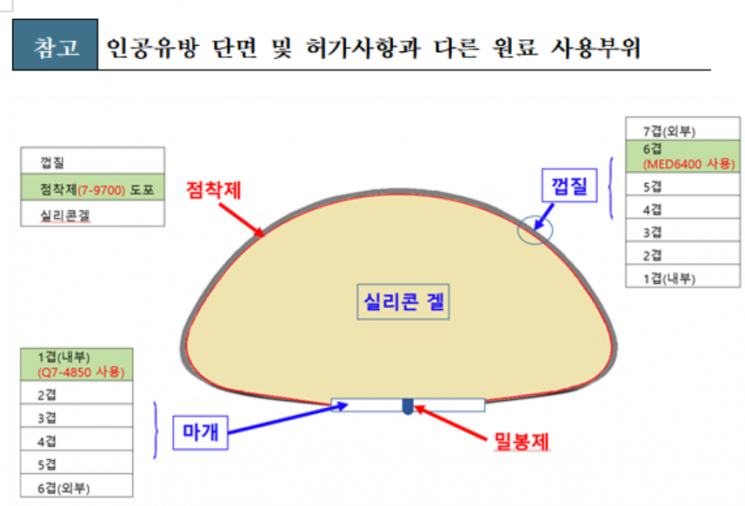
실리콘 겔 인공유방은 유방을 재건하거나 성형하는 데 사용되는 제품으로, 실리콘 주머니 안에 실리콘 겔이 포함된 제품이다.
식약처의 점검 결과 한스바이오메드는 2015년 12월부터 허가사항과 다른 원료를 사용해 부적합한 인공유방을 생산하고 약 7만여개를 의료기관에 공급했다.
허가사항에 기재되지 않은 원료는 총 5종이다. 이 중 실리콘점착제는 피부접촉 의료기기(상처보호제)에, 나머지 4종은 국내 허가된 다른 인체이식 의료기기(인공유방, 심장판막 등)에 사용되는 원료다.
전문가들은 허가사항에 기재되지 않은 원료 5종은 대부분 다른 이식 의료기기에 사용되는 만큼 정상적 상태에서 누출 가능성이 매우 적어 이식환자에 미칠 위험성은 낮다고 봤다. 식약처는 다만 이식환자에 대한 지속적인 모니터링이 필요하다고 판단했다.
또 인공유방 제조공정 중 고온 환경에서 발생 가능하다고 알려진 기체 '포름알데히드'는 이후 내부 공기제거 과정을 거쳐 제품에는 잔류 가능성이 적다는 전문가의 견해가 있었다. 식약처의 완제품 포름알데히드 잔류시험 결과 이 제품에서는 검출되지 않았다.
식약처는 해당 품목에 대한 판매중지와 회수를 명령하고 성형학회, 의사협회 등 관련 단체를 통해 의료기관에 해당 제품의 사용을 중지하도록 요청했다. 한스바이오메드에는 의료기기법 위반으로 업무정지 등 행정처분을 할 예정이다.
식약처는 해당 제품을 시술받은 환자들의 안전?안심을 위해 ▲ 신속한 환자 파악 ▲안전성 정보 제공 ▲전담 소통창구 마련 ▲이식환자 장기 모니터링 ▲보상방안 등을 추진한다.
이를 위해 현재 해당 제품을 이용해 유방재건술을 실시한 환자 현황을 파악 중이다. 식약처는 개별 이식환자에게 정기검사 항목, 진단절차, 환자 대처요령 등 정보를 의료기관을 통해 제공할 방침이다.
꼭 봐야 할 주요 뉴스
!["지금부터 주가 2배 이상 뛴다" 데이터센터 지을때마다 웃는 이 종목 [클릭 e종목]](https://cwcontent.asiae.co.kr/asiaresize/93/2026050416112750184_1777878687.jpg) "지금부터 주가 2배 이상 뛴다" 데이터센터 지을때...
"지금부터 주가 2배 이상 뛴다" 데이터센터 지을때...
식약처는 한스바이오메드에 이식환자에 대한 보상방안 마련하여 제출하도록 한 상태다. 진단·검사비, 부작용 시 보상대상·범위·기간을 조속히 확정하도록 할 계획이다. 또 다양한 분야의 전문가와 논의해 환자 장기 모니터링 등 계획을 수립하고 그 결과를 분석·평가할 예정이다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>







![[디펜스칼럼]만성적자 군인연금 이젠 결정해야](https://cwcontent.asiae.co.kr/asiaresize/308/2026050607072481066A.jpg)
![[초동시각]전세소멸, 거스를 것인가 대비할 것인가](https://cwcontent.asiae.co.kr/asiaresize/308/2026050611180507067A.jpg)
![[산업의 맥]AI 에이전트 커머스와 디지털 화폐](https://cwcontent.asiae.co.kr/asiaresize/308/2026050609553456901A.jpg)






!["비트코인 무조건 보유" 스트래티지가 변했다…필요시 매도 [비트코인 지금]](https://cwcontent.asiae.co.kr/asiaresize/308/2026031809441379682_1773794653.jpg)
![[실전재테크]AI 타고 뜨는 광통신·장비株…옥석가리기 필요](https://cwcontent.asiae.co.kr/asiaresize/308/2026050608142696187A.jpg)
![[실전재테크]'에이전트AI 시대' 주목받는 CPU…투자 유망 종목은](https://cwcontent.asiae.co.kr/asiaresize/308/2026050607510850837_1778021468.png)





![7거래일 연속 신고가, 진짜 이유 따로 있었다…美 AI데이터센터 투자 급증에 웃는 LS일렉트릭[이주의 관.종]](https://cwcontent.asiae.co.kr/asiaresize/309/2026050413571549947_1777870634.jpg)




![[속보]'김건희 항소심 재판' 신종오 판사, 법원서 숨진 채 발견](https://cwcontent.asiae.co.kr/asiaresize/309/2026050422131350385_1777900394.png)
![오세훈, 밝히고 싶지 않은 신체의 비밀…연수원 1년 더 다닌 사연[시사쇼]](https://cwcontent.asiae.co.kr/asiaresize/309/2026050610420551392_1778031726.jpg)








