삼성바이오에피스, 스텔라라 시밀러 유럽 허가 '청신호'
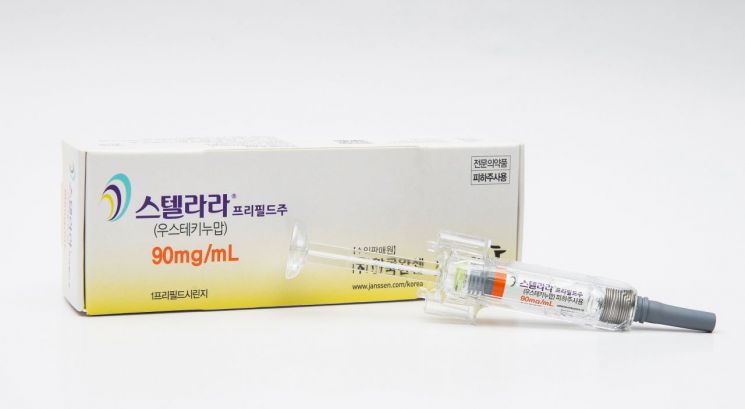
삼성바이오에피스는 유럽의약품청(EMA) 산하 약물사용자문위원회(CHMP)로부터 자가면역질환 치료제 스텔라라의 바이오시밀러로 개발한 피즈치바(개발명 SB17)에 대한 판매 허가 긍정 의견을 획득했다고 25일 밝혔다.
유럽연합(EU)은 의약품에 대한 과학적 평가를 토대로 의약품 허가에 대한 의견을 제시하는 EMA 산하 CHMP가 허가 권고를 내린 약물에 대해 EU 집행위원회(EC)가 2~3개월 이내에 의약품의 최종 판매 허가를 내리는 방식으로 새로운 의약품을 승인한다. 이로써 피즈치바는 유럽 내 판매를 위한 9부 능선을 넘은 셈이다. 지난해 글로벌 제약사 산도스와 피즈치바의 유럽 및 북미 판매를 위한 파트너십 계약을 맺은 상태로 이에 따라 향후 유럽 내 판매는 산도스가 맡을 예정이다.
피즈치바의 오리지널 의약품인 스텔라라는 존슨앤드존슨(J&J)이 개발한 판상 건선, 건선성 관절염, 크론병 등의 자가면역질환 치료에 쓰는 약이다. 지난해에만 세계에서 108억5800만달러(약 14조5000억원)의 매출을 올린 블록버스터 의약품이다. 자가면역질환은 우리 몸속 면역체계가 외부의 적이 아닌 몸속의 정상세포를 적으로 잘못 인식해 공격하는 병이다. 이 과정에서 백혈구에서 분비돼 면역세포를 활성화하는 단백질 중 하나가 인터류킨이다. 스텔라라는 이 중 인터류킨-12, 23의 활성을 억제해 자가면역질환을 치료한다.
삼성바이오에피스는 현재 유럽 시장에서 총 7종의 바이오시밀러 제품을 상업화했고, 이 중 3종은 스텔라라와 유사한 자가면역질환 치료제 엔브렐·레미케이드·휴미라의 바이오시밀러다. 이들 바이오시밀러들은 종양괴사인자(TNF)-알파(α)를 억제해 자가면역질환을 치료하는 기전을 가졌다. 이번 피즈치바의 허가 긍정 의견 획득으로 삼성바이오에피스는 자가면역질환 치료제 포트폴리오를 한 층 더 확장할 수 있게 됐다.
꼭 봐야 할 주요 뉴스
!["이제 부동산은 한 물 갔어요"…100억 자산가도 건물 팔아 주식한다[부자들의 투자전략]①](https://cwcontent.asiae.co.kr/asiaresize/93/2026050406591149045_1777845551.jpg) "이제 부동산은 한 물 갔어요"…100억 자산가도 건...
"이제 부동산은 한 물 갔어요"…100억 자산가도 건...
정병인 삼성바이오에피스 규제업무(RA)팀장(상무)은 "삼성바이오에피스의 첫 인터류킨 억제 기전 약물인 피즈치바의 유럽 허가 권고를 받아 기쁘다"며 "앞으로 다양한 파이프라인 확보를 통해 환자들에게 더 많은 치료 옵션을 제공할 수 있도록 노력하겠다"고 말했다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>
![삼성바이오에피스 사옥 전경[사진제공=삼성바이오에피스]](https://cphoto.asiae.co.kr/listimglink/1/2021012508561742259_1611532577.jpg)


![[초동시각]값싼 용서와 소년범죄](https://cwcontent.asiae.co.kr/asiaresize/308/2026043011072981168A.jpg)
![[기자수첩]쿠팡이 던진 과제, 40년 묵은 '동일인 제도' 손볼 때 됐다](https://cwcontent.asiae.co.kr/asiaresize/308/2026043009314852085A.jpg)
![[수담(手談)] 과거에 묶인 자, 미래를 두는 자](https://cwcontent.asiae.co.kr/asiaresize/308/2026043011074583292A.jpg)
!["배움은 최고의 노화방지"…90대는 돼야 '화석 학번' 되는 日의 시니어 대학[日요일日문화]](https://cwcontent.asiae.co.kr/asiaresize/308/2026042915352045725_1777444520.png)






!["그냥 비염 아니었다"…석 달째 코막힘 '이것' 때문이었다니[콕!건강]](https://cwcontent.asiae.co.kr/asiaresize/308/2026043016511147805_1777535471.png)






![편의점 커피는 동서식품, 캡슐은 네슬레?…스타벅스 로고의 진실[맛잘알X파일]](https://cwcontent.asiae.co.kr/asiaresize/309/2025072310081756151_1753232897.jpg)





![“AI가 야근하면 메모리도 밤샌다”…삼성전자·SK하이닉스 웃는 이유[주末머니]](https://cwcontent.asiae.co.kr/asiaresize/309/2025092314141644857_1758604457.png)


!["배움은 최고의 노화방지"…90대는 돼야 '화석 학번' 되는 日의 시니어 대학[日요일日문화]](https://cwcontent.asiae.co.kr/asiaresize/309/2026042915352045725_1777444520.png)







