식약처, 바이오헬스 분야 '제품화전략지원단' 출범
공공성·산업적 가치 높은 제품 우선 지원
제품화지원팀·혁신제품심사팀·임상심사팀
비임상·임상 설계 및 상담 지원…심사 신속화
[아시아경제 김영원 기자] 식품의약품안전처가 바이오헬스 제품 개발을 처음부터 끝까지 맡는 전담 지원단을 만든다.
식약처는 공중보건 위기대응 의약품, 신개념·신기술 의약품의 신속한 시장 진입을 지원하고 바이오헬스 산업을 육성하기 위해 '제품화전략지원단'을 출범한다고 25일 밝혔다.
식약처는 그동안 의약품(팜나비), 바이오의약품(마중물), 의료기기(허가 도우미) 등 제품 분야별로 제품화 지원 사업을 운영해왔다. 규제 상담은 2020년 8월 신설된 상담 전담 부서인 '사전상담과'가 맡아 진행해왔다.
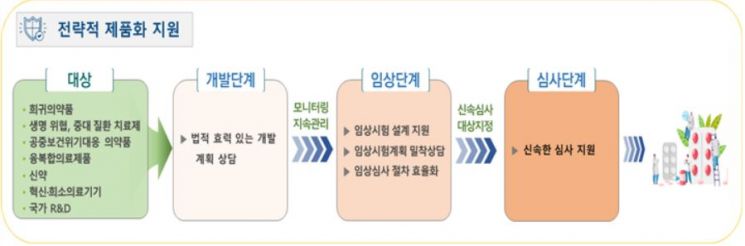
지원단은 '개발-비임상', '임상-허가심사'의 연계와 임상시험 설계에 대한 전문 서비스 등을 제공한다. 개발 단계별로 진입 속도를 빠르게 하기 위해 지원 기능이 강화됐다.
공공성이 높거나 산업적 가치가 높은 제품이라고 판단되면 우선 지원 대상이다. 공중보건 위기 대응 의약품, 희귀 의약품, 국내 개발 신약, 혁신 의료기기, 신기능성 식품 원료 등이다. 지원단은 이들을 우선 지원하고 향후 대상을 점차 확대할 계획이다.
지원단의 단장은 식품의약품안전평가원장이 맡는다. 팀 구성은 제품화지원팀, 혁신제품심사팀, 임상심사팀 총 3개로 구성되며, 인원은 총 90명이다.
제품화지원팀은 품질, 비임상, 임상에 대한 심층 상담을 맡았다. 또 인허가 심사자료를 준비하기 어려운 신기술 제품은 각 심사부서와 논의해 규제 서비스를 제공하기도 한다.
혁신제품심사팀은 개발 단계부터 '신속심사 대상' 제품을 선택하고, 개발이 완료된 제춤의 허가 기간을 단축하기 위해 '수시동반심사' 프로그램을 운영한다. 수시동반심사란 유망한 치료제를 최종 허가 단계에서 심사하는 것이 아닌, 임상 등 진행 단계마다 수시로 자료를 받아 검토하는 것이다.
임상심사팀은 (비)임상자료, 임상시험 계획을 심사하고 제품화지원팀의 상담과 연계해 임상 상세설계를 돕는다.
꼭 봐야 할 주요 뉴스
!["지금부터 주가 2배 이상 뛴다" 데이터센터 지을때마다 웃는 이 종목 [클릭 e종목]](https://cwcontent.asiae.co.kr/asiaresize/93/2026050416112750184_1777878687.jpg) "지금부터 주가 2배 이상 뛴다" 데이터센터 지을때...
"지금부터 주가 2배 이상 뛴다" 데이터센터 지을때...
김강립 식약처장은 "시장진입 단계의 규제를 국제기준과 조화시키고 불확실성을 완화해 우리 기업들이 국제적인 규제 수준을 넘어 글로벌 시장으로 나아가기 위한 환경을 조성하도록 노력하겠다"고 말했다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>







![[디펜스칼럼]만성적자 군인연금 이젠 결정해야](https://cwcontent.asiae.co.kr/asiaresize/308/2026050607072481066A.jpg)
![[초동시각]전세소멸, 거스를 것인가 대비할 것인가](https://cwcontent.asiae.co.kr/asiaresize/308/2026050611180507067A.jpg)
![[산업의 맥]AI 에이전트 커머스와 디지털 화폐](https://cwcontent.asiae.co.kr/asiaresize/308/2026050609553456901A.jpg)






!["비트코인 무조건 보유" 스트래티지가 변했다…필요시 매도 [비트코인 지금]](https://cwcontent.asiae.co.kr/asiaresize/308/2026031809441379682_1773794653.jpg)
![[실전재테크]AI 타고 뜨는 광통신·장비株…옥석가리기 필요](https://cwcontent.asiae.co.kr/asiaresize/308/2026050608142696187A.jpg)
![[실전재테크]'에이전트AI 시대' 주목받는 CPU…투자 유망 종목은](https://cwcontent.asiae.co.kr/asiaresize/308/2026050607510850837_1778021468.png)





![7거래일 연속 신고가, 진짜 이유 따로 있었다…美 AI데이터센터 투자 급증에 웃는 LS일렉트릭[이주의 관.종]](https://cwcontent.asiae.co.kr/asiaresize/309/2026050413571549947_1777870634.jpg)



![[속보]'김건희 항소심 재판' 신종오 판사, 법원서 숨진 채 발견](https://cwcontent.asiae.co.kr/asiaresize/309/2026050422131350385_1777900394.png)

![오세훈, 밝히고 싶지 않은 신체의 비밀…연수원 1년 더 다닌 사연[시사쇼]](https://cwcontent.asiae.co.kr/asiaresize/309/2026050610420551392_1778031726.jpg)








