식약처 "美 코오롱티슈진 현지실사"…이르면 6월 허가취소 결정(종합)
'부실검증' 논란에 첨단바이오의약품 제도 손질…환자 3400명 장기추적조사
[아시아경제 서소정 기자] 보건당국이 성분 논란이 불거진 골관절염 치료제 '인보사케이주'에 대해 개발사인 미국 코오롱티슈진 코오롱티슈진 close 증권정보 950160 KOSDAQ 현재가 103,600 전일대비 1,200 등락률 -1.15% 거래량 458,709 전일가 104,800 2026.05.06 15:30 기준 관련기사 코스피, 7300선 장 마감 '최고치'…6%대 급등 코스피, 장중 7400선 위로…'27만전자' 도달(상보) 코스피 7300 뚫었는데 코스닥은 왜…시총 상위종목 대부분 하락세 을 직접 현지실사해 세포가 바뀐 경위 등을 조사키로 했다. 식약처는 인보사 성분 논란 진위를 밝히기 위한 자체 시험검사를 이달 중순부터 다음달 말까지 진행하고 이르면 6월 허가취소 여부를 결정할 계획이다.
15일 식품의약품안전처는 코오롱생명과학 코오롱생명과학 close 증권정보 102940 KOSDAQ 현재가 59,400 전일대비 200 등락률 -0.34% 거래량 35,034 전일가 59,600 2026.05.06 15:30 기준 관련기사 코오롱생명과학, 항암 유전자치료제 KLS-3021 전임상 결과 국제학술지 게재 코오롱바이오텍, '바이오 코리아 2026' 참가…CDMO 경쟁력 알린다 코오롱생명과학 "TG-C 혼합세포 유전자 요법, 아시아 특허" 인보사 관련 중간조사 결과를 발표하고, 인보사의 수거·검사 결과 국내에 사용된 세포도 미국에서 사용된 세포와 마찬가지로 주성분 중 2액이 허가 당시 제출한 자료에 기재된 연골세포가 아닌 신장세포인 것으로 확인됐다고 밝혔다. 식약처는 코오롱생명과학의 자회사인 미국 코오롱티슈진에 대한 현지실사를 통해 최초 개발단계부터 신장세포였는지 여부 등을 확인할 계획이다.
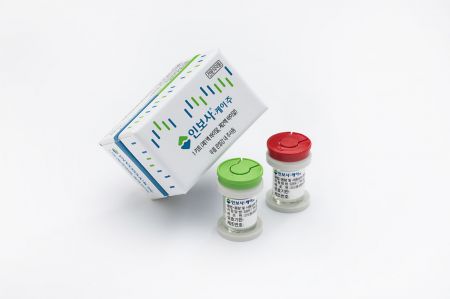
◆"국내 제품도 미국처럼 연골 아닌 신장세포"= 인보사는 중증도 무릎 골관절염의 치료에 사용되는 유전자치료제로, 주성분은 1액(동종유래 연골세포)과 2액(TGF-β1 유전자삽입 동종유래 연골세포)으로 구성된다. 하지만 코오롱 측이 뒤늦게 인보사의 주성분 중 1개 성분(2액)이 허가 당시 제출자료에 기재된 세포와 다른 세포로 추정된다고 보고하자 식약처는 지난달 31일부터 해당 제품의 제조·판매를 중지한 상황이다.
식약처 관계자는 "식약처가 제조용 세포주 등을 수거해 유전학적 계통검사(STR)를 실시한 결과 코오롱의 자체 검사와 동일하게 2액 세포가 신장세포임을 확인했다"고 말했다.
이에 따라 식약처는 현재 시판중인 제품(2액)의 주성분이 신장세포로 바뀐 경위와 이유 등에 대해 추가로 조사를 실시키로 했다. 식약처는 ▲2액 주성분이 신장세포로 바뀐 경위와 그 과정을 입증하는 과학적 근거 ▲2액 주성분이 신장세포로 바뀌었으나 이를 연골세포라고 허가신청한 경위 ▲당초 연골세포로 생각됐던 2액 주성분에 대한 최초의 개발계획 ▲2액 주성분의 제조·생산·확인과 관련된 일체의 자료 ▲독성시험 등의 결과가 연골세포에 대한 것인지, 신장세포에 대한 것인지 등을 코오롱 측에 자료로 제출할 것을 명령했다.
식약처 관계자는 "코오롱이 제출한 자료와 식약처 자체 시험검사 결과, 미국 현지실사 결과 등을 종합적으로 판단해 사실관계를 명확하게 확인하고, 그에 상응하는 행정처분 등 필요한 조치를 취할 것"이라면서 "자체 검사 등 시일이 소요돼 행정처분 등 결과가 나오려면 최소한 6월경은 돼야할 것"이라고 말했다.
◆첨단바이오 의약품 검증 절차 강화= 식약처와 코오롱 측은 이미 해당 제품을 투여받은 환자의 안전을 확보하기 위해 투여환자 전체에 대한 특별관리 및 장기추적조사를 실시할 계획이다. 우선 한국의약품안전관리원을 통해 그간 투여환자의 병력 등 관련 자료를 분석해 연내까지 이상반응을 파악하고, 인보사를 특별관리 대상으로 지정해 투여환자를 위한 전담소통창구를 운영하기로 했다. 허가 후 투여건수는 지난달 30일 기준 3707건이다.
식약처는 이번사건을 계기로 유전자치료제 등 첨단바이오의약품에 대한 관리제도 개선에 나선다. 허가 전부터 세포관리를 강화하기 위해 ‘인체세포 등 관리업’을 신설해 세포의 채취부터 처리·보관·공급에 이르기까지 단계별로 안전 및 품질관리기준을 마련할 계획이다. 허가 신청 시에는 연구개발과 제조 등에 사용된 모든 세포에 대한 ‘유전학적 계통검사(STR)’ 결과를 의무적으로 제출하도록 하고, 허가 과정에서 중요한 검증요소는 식약처가 교차 검증해 세포의 동일성을 확인할 계획이다.
식약처 관계자는 "허가 이후에도 업체가 주기적으로 유전자 검사를 실시하고, 검사결과를 보관하도록 하는 등 사후관리를 강화할 예정"이라며 "세포·유전자치료제 등에서 만일에 발생할 지도 모르는 부작용에 대비하기 위해 장기추적조사를 의무화할 방침"이라고 말했다.
다음은 인보사 성분 논란과 관련한 식약처 일문일답.
-식약처가 허가 사항과 다른 세포임을 알게 된 경위는
▲코오롱생명과학은 3월 22일 미국에서 임상시험 제품에 대해 자체적으로 유전자 검사를 진행했으며, 해당 세포 변경가능성이 있다는 것을 식약처에 보고해 처음 알게 됐다. 국내에서 제조된 2액 제품과 원료(제조용 세포주)에 대한 식약처의 유전학적 계통 (STR) 검사 결과에서도 당초 연골세포가 아닌 신장세포임이 확인됐다.
-미 FDA가 임상과정에서 문제 가능성을 인지하고 시험을 권고했나
▲해당 시험은 코오롱티슈진이 미국 허가 준비 과정 중 자체적으로 검사를 실시한 것이다. 최종검사 결과를 3월 30일에 미 FDA에 공식 통지한 것으로 코오롱생명과학에 대한 현장실사 시 확인했다. 식약처는 4월 2일에 주미 한국대사관을 통해 미 FDA에 공식 질의해 확인 중에 있다.
-인보사 허가심사시 연골세포로 판단한 근거는
▲허가 당시 코오롱생명과학이 제출한 자료는 2액의 세포가 연골세포임을 보여주고 있고, 신장세포로 판단할 수 있는 근거는 없었다. ①2액 세포에서 나타나는 단백질 및 유전자의 양상이 ‘연골세포’와 유사 ②2액 세포의 DNA 지문분석 결과 ‘연골세포’의 DNA 분포 패턴(양상)이 유사 ③연골세포에서 주로 나타나는 표면단백질이 2액에서도 확인 ④2액을 투여한 동물에게서 연골이 재생된 것을 확인 등을 검토해 연골세포라고 판단했다. 이런 결과는 전문가 위원회를 통해서도 확인됐다.
-식약처 허가시 검토결과와 오늘 중간검사결과가 차이 나는 이유는
▲지금까지 업체는 초기 연구개발과정에서 2액의 제조과정 중 신장세포가 분리·정제 미비로 혼입돼 당초 만들려던 연골세포를 신장세포가 대체하게 됐다고 추정하고 있다. 현재 식약처는 국내에서 사용한 세포가 신장세포임을 최종확인 후 업체에 경위 및 그 과정을 입증하는 과학적 근거 등에 대한 자료제출을 15일 명령했고, 세포 유전자 검사 등을 추가로 진행하고 있다. 앞으로 식약처는 업체가 제출한 자료, 식약처 자체 시험검사 결과, 미국 현지실사 결과 등을 종합적으로 판단해 사실관계를 명확하게 확인하고 세포가 바뀐 경위를 확인할 계획이다.
-추가 조사 계획은
▲식약처는 2액의 주성분이 신장세포로 바뀐 이유 및 경위 등을 추가로 조사할 계획이다. 또 인보사의 개발사인 미국 코오롱티슈진과 세포은행인 바이오릴라이언스사와 위시사에 대한 현지실사 결과 등을 통해 최초 개발 단계부터 신장세포였는지 여부 등을 확인할 계획이다.
꼭 봐야 할 주요 뉴스
 "집에 처박혀있나 나도 찾아볼까?"…누가 아재 취...
"집에 처박혀있나 나도 찾아볼까?"…누가 아재 취...
-인보사 종양발생 가능성과 향후 환자 안전 대책은
▲지금까지 수집된 이상사례에 따르면 약물과 인과관계가 확인된 종양 발생 사례는 없었다. 허가 시 연골세포임을 전제로 종양원성시험을 통해 종양가능성이 없음을 확인했고, 제조 과정에서 2액에 방사선을 조사하고 44일내 사멸하는지 확인한 뒤 투여하도록 했다. 다만 주성분이 허가사항과 다른 세포로 확인됨에 따라 안전성 측면에서 추가적인 고려사항이 있는지 확인할 예정이다. 현재 수거·검사를 통해 2액의 세포사멸 확인시험을 5월 말 완료할 예정이며, 투여받은 모든 환자에 대해 15년간 장기추적조사를 실시할 계획이다.
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>







![[디펜스칼럼]만성적자 군인연금 이젠 결정해야](https://cwcontent.asiae.co.kr/asiaresize/308/2026050607072481066A.jpg)
![[초동시각]전세소멸, 거스를 것인가 대비할 것인가](https://cwcontent.asiae.co.kr/asiaresize/308/2026050611180507067A.jpg)
![[산업의 맥]AI 에이전트 커머스와 디지털 화폐](https://cwcontent.asiae.co.kr/asiaresize/308/2026050609553456901A.jpg)






!["비트코인 무조건 보유" 스트래티지가 변했다…필요시 매도 [비트코인 지금]](https://cwcontent.asiae.co.kr/asiaresize/308/2026031809441379682_1773794653.jpg)
![[실전재테크]AI 타고 뜨는 광통신·장비株…옥석가리기 필요](https://cwcontent.asiae.co.kr/asiaresize/308/2026050608142696187A.jpg)
![[실전재테크]'에이전트AI 시대' 주목받는 CPU…투자 유망 종목은](https://cwcontent.asiae.co.kr/asiaresize/308/2026050607510850837_1778021468.png)





![7거래일 연속 신고가, 진짜 이유 따로 있었다…美 AI데이터센터 투자 급증에 웃는 LS일렉트릭[이주의 관.종]](https://cwcontent.asiae.co.kr/asiaresize/309/2026050413571549947_1777870634.jpg)


![[속보]'김건희 항소심 재판' 신종오 판사, 법원서 숨진 채 발견](https://cwcontent.asiae.co.kr/asiaresize/309/2026050422131350385_1777900394.png)

![오세훈, 밝히고 싶지 않은 신체의 비밀…연수원 1년 더 다닌 사연[시사쇼]](https://cwcontent.asiae.co.kr/asiaresize/309/2026050610420551392_1778031726.jpg)









