韩国全球医药产业协会(KRPIA)研究结果
[亚洲经济 记者 Lee Myeonghwan] 国内新药的许可及审评所需时间平均约为314天。
韩国全球医药产业协会(KRPIA)16日表示,协会以过去10年(2011~2020年)在韩国获批的全球制药企业235个新药为对象,开展了题为“韩国新药许可周期调查研究”的项目,并公布了上述结果。
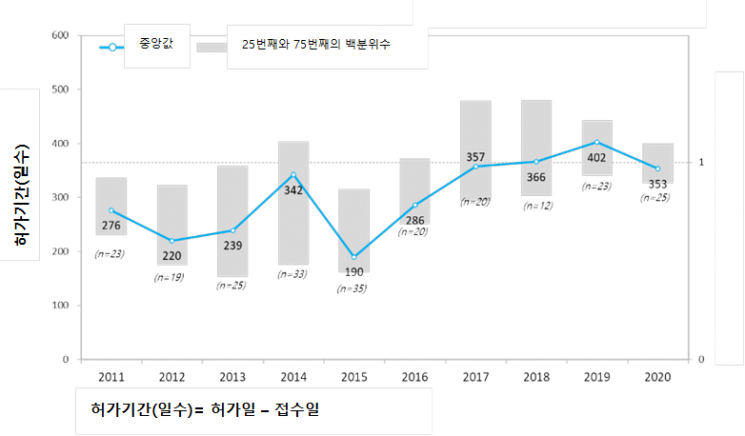
根据本次调查研究结果,在调查期间,新药获批及审评所需时间平均为313.7天,自2015年以后呈持续增加趋势。与截至2017年的调查结果——平均299.7天相比,增加了约2周。
按药品类型来看,化学合成药平均为291.0天,生物医药品为353.0天。回归分析结果显示,与化学合成药相比,生物医药品平均多耗时43.2天。
在按新药适应症分类的比较分析中,抗癌药的获批数量最多,共92件(39.1%)。各适应症之间的审评周期差异不大,但抗癌药的许可及审评时间相对更快。
占全部新药37.4%的罕见病用药截至2020年共有88个品种获批。统计显示,罕见病用药从申报到获批所需时间平均比普通品种快130.4天。
但尽管为促进罕见病药物开发并强化患者可及性,于2015年制定了《罕见疾病管理法》,自2016年以后罕见病用药的许可及审评时间仍出现延长。由于罕见病用药需经过单独的罕见病药物指定程序,将其纳入在内的全部民愿审查所需时间进一步拉长。说明称,这是多重因素共同作用的结果,包括自2015年7月1日以后实施的罕见病用药生产及质量管理规范(GMP)审查和引入风险管理计划、生物医药品数量增加等。
协会解释称,通过本次研究发现,在许可及审评过程中,GMP审查所需时间平均比安全性、有效性审查或标准及检验方法审查更长。尤其是是否进行GMP现场核查及其时间安排,以及由此产生的审查周期,对整体许可审评时间产生了较大影响。
另一方面,说明指出,2020年尽管处于新冠肺炎疫情暴发初期,许可审评时间却较前一年有所缩短。有分析推测,这一时期对生产场所免予现场核查是主要原因。
协会表示:“随着2021年7月20日《药师法》修订,为改进优先审评、附条件许可等快速许可和审评制度作出了多方面努力”,但同时指出,“要缩短许可所需时间,仍有必要在持续扩充审评部门专业人力、推动相关规定与国际接轨并加强与外国监管机构的合作、扩大互认制度等方面继续努力”。
版权所有 © 阿视亚经济 (www.asiae.co.kr)。 未经许可不得转载。

![“有钱也享受不到”……真正“顶级0.1%”的世界 [奢华世界]](https://cwcontent.asiae.co.kr/asiaresize/93/2026051507261063923_1778797570.png)







