持续增长的SaMD,临床批准数量一年内翻倍
[亚洲经济 记者 Lee Chunhee] 去年,国内软件医疗器械(SaMD)的开发尝试增多,同时其针对的目标疾病也呈现多样化趋势。
食品医药品安全处于13日公开了包含上述内容在内的数字治疗(辅助)器械(DTx)等 SaMD 去年临床试验计划获批情况以及各领域获批产品现状。SaMD 是仅通过软件开发、制造并获得许可、认证或完成申报的医疗器械,大致分为▲疾病“诊断辅助·预测”▲疾病·症状“治疗·缓解”(DTx)▲“手术治疗·辅助”三大领域。
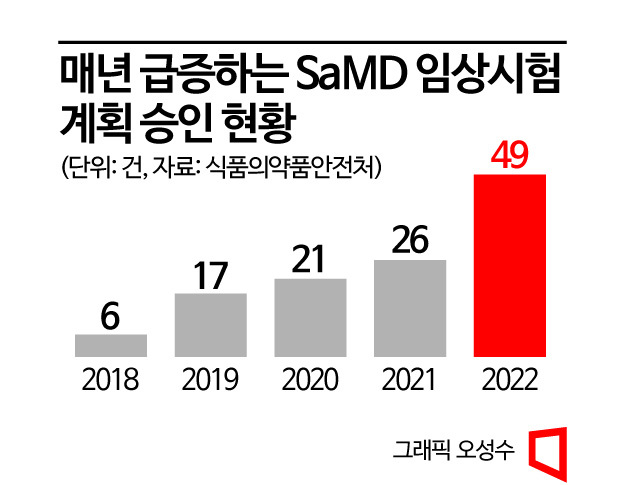
SaMD 临床试验计划获批件数近期呈现逐年激增的态势。自2018年起至去年这5年间,从6件增加到49件,增长逾8倍。尤其是去年达到49件,较前年的26件几乎翻倍。从领域来看,以人工智能(AI)为基础的软件等诊断辅助·预测领域以31件位居首位,其次为 DTx 17件,增强现实(AR)基础的手术辅助软件等手术·治疗·辅助领域为1件。
在诊断辅助·预测领域,利用AI对脑部计算机断层扫描(CT)影像进行分析,用于急性脑梗塞发生与否及发生部位的诊断辅助、在超声影像中辅助检出胰腺癌区域、分析心血管疾病患者的病历记录以预测其在1年内发生心肌梗塞风险的产品等,已获得批准。
在 DTx 领域,2021年有9项临床试验针对8种疾病获批,而去年有17项临床试验针对12种疾病获批,呈现出数量与质量双重提升。以游戏为基础,用于改善已被诊断为注意力缺陷多动障碍(ADHD)的小儿患者的注意力缺陷,分析轻度认知障碍(MCI)患者的认知状态并提供认知治疗方法以改善认知功能的产品等获得了批准。食品医药品安全处相关负责人表示:“此前 DTx 领域的产品开发以缓解失眠或成瘾症状为主流”,并解释称,“相比之下,去年可以确认到已经开始尝试将其应用于 ADHD、MCI、发育障碍等更多样的疾病。”
从临床阶段来看,前期临床的探索性临床有16件,后期临床的确证性临床有33件,数量更多。与通常按第1~3期划分实施的药品临床试验不同,医疗器械分为探索性临床和确证性临床两次临床试验来实施。探索性临床是针对少量受试者在相对较短时间内实施的临床试验,而确证性临床则是为确保统计学显著性,招募更多受试者开展的临床试验。不过,食品医药品安全处表示:“其中已结束的临床试验有9件,正在进行中的有18件,尚未启动的有22件”,“预计这些产品真正应用到医疗现场还需要更多时间。”
版权所有 © 阿视亚经济 (www.asiae.co.kr)。 未经许可不得转载。
![“有钱也享受不到”……真正“顶级0.1%”的世界 [奢华世界]](https://cwcontent.asiae.co.kr/asiaresize/93/2026051507261063923_1778797570.png)







