SK바사 'GBP510' 국내 첫 임상 3상 성공
후속 개발에도 청신호
유바이오로직스·셀리드
진원생명과학·큐라티스 등
8개 업체 백신 개발 경쟁
유바이오 '유코백-19'
임상 3상 올해 3분기 내 마무리 구상
국산 2호 백신으로 가장 유력

SK바이오사이언스의 코로나19 백신 'GBP510'
[아시아경제 이춘희 기자] SK바이오사이언스 의 ‘GBP510’이 국내 개발 코로나19 백신 중 처음으로 임상3상을 성공함에 따라 지지부진했던 후속 국산 백신 개발에도 청신호가 켜졌다. 국산 2호 백신 개발에 성공하는 업체가 어느 곳이 될지에도 관심이 쏠린다.
유바이오 등 줄줄이 임상
27일 식품의약품안전처에 따르면 코로나19 백신 개발을 추진하고 있는 곳은 총 8곳이다. SK바이오사이언스에 이어 유바이오로직스 , 셀리드 , 진원생명과학 , 큐라티스, HK이노엔 , 아이진 , 에스티팜 등이 국산 2호 코로나19 백신을 노리고 있다.
다음 타자로 가장 유력한 것은 유바이오로직스의 ‘유코백-19’다. GBP510을 제외하면 국내 개발 백신 중 유일하게 임상3상 진입에 성공했다. 지난 1월 식품의약품안전처로부터 한국, 필리핀, 방글라데시 등에서 4000명 규모의 다국가 임상3상을 승인받았다. 회사 측은 올해 3분기 내로 해외 지역은 임상3상을 마친다는 구상이다. 셀리드도 ‘AdCLD-COV19’의 임상 2b·3상 동시 신청을 노렸지만 식약처와 협의 끝에 2b상만 우선 진행하고 추후 3상을 별도 제출하기로 했다.
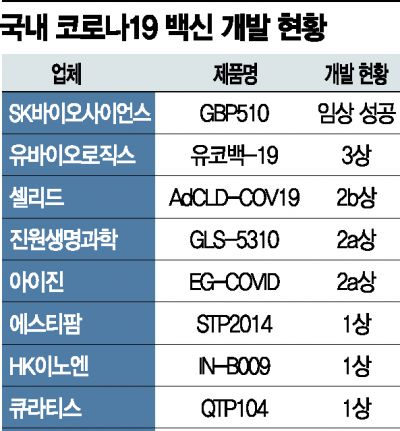
차세대 백신으로 주목받고 있는 메신저리보핵산(mRNA) 기술을 토대로 한 백신 개발도 이뤄지고 있다. 에스티팜(STP2014), 아이진(EG-COVID), 큐라티스(QTP104) 등이 mRNA 코로나19 백신 개발을 추진하고 있다. 특히 에스티팜은 한미약품, GC 녹십자 , 동아에스티 등과 함께 ‘K-mRNA 컨소시엄’을 구성했다. 또 아이진, 큐라티스, 진원생명과학 등 3사가 기술 개발을 맡고 보령바이오파마가 위탁생산(CMO)하는 구조의 ‘mRNA 바이오벤처 컨소시엄’이 꾸려지면서 두 컨소시엄의 시장 선점을 위한 경쟁도 이뤄지고 있다.
추가접종 전용 백신으로 전환하는 기업도 나타났다. 진원생명과학은 ‘GLS-5310’의 기존 임상2a상을 축소하고, 이를 통해 확인한 안전성과 유효성을 토대로 추가접종 전용 백신으로 2b·3상을 진행하기로 했다. 박영근 진원생명과학 대표는 "기존 코로나19 백신들의 재접종 시 예방 효능에 한계가 보고되고 매년 백신을 접종해야 할 가능성도 예상된다"고 설명했다. 진원생명과학은 치료제 ‘GLS-1027’의 2상도 진행 중이다. SK바이오사이언스 역시 GBP510의 추가접종·교차접종을 위한 임상을 진행 중이다.
GBP510 성공, 후속 백신개발에 기폭제
GBP510의 성공은 다른 백신들의 개발에도 긍정적인 영향을 미칠 전망이다. 인체 임상은 대상 약품을 투여한 실험군과 식염수 등의 위약을 투여한 대조군 간의 비교를 통해 이뤄진다. 하지만 팬데믹(세계적 대유행) 상황에서 위약의 투여가 어려운 만큼 현재 국내 임상3상은 대조군에 위약이 아닌 기존 허가 백신을 대조백신으로 접종하고, 임상 데이터를 비교한 후 비열등성을 입증하는 방식으로 이뤄지고 있다. GBP510 역시 아스트라제네카(AZ) 백신을 대조백신으로 활용해 임상3상을 진행했다.
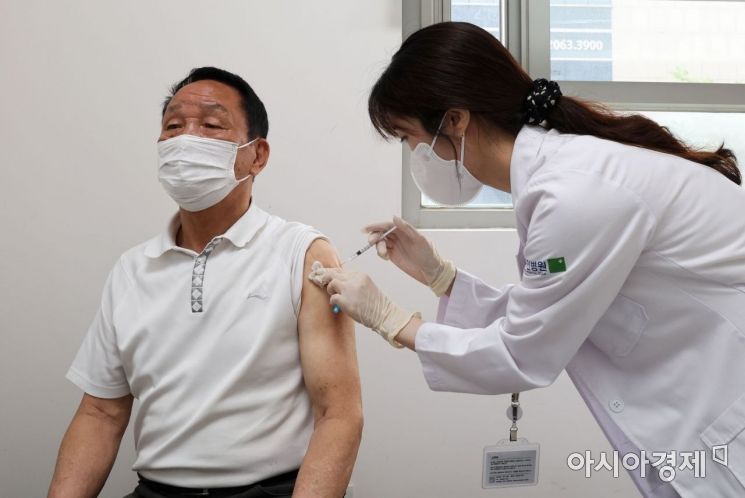
60세 이상 사전예약자에 대한 코로나19 4차 예방접종이 시작된 지난 25일 서울 강서구 부민병원에서 한 시민이 백신을 접종하고 있다. 2022. 4. 25 사진공동취재단 (초상권 동의 얻음)
하지만 해외에서 개발된 백신을 대조백신으로 활용하기는 현실적으로 어렵기 때문에 많은 국내 기업들이 임상3상 진행에 난항을 겪어 왔다. SK바이오사이언스도 AZ 백신을 기존에 CMO했던 관계와 정부 등의 지원이 없었다면 대조백신 확보가 어려웠을 것이라는 게 업계의 중론이다. 유바이오로직스 역시 해외에서는 AZ 백신을 대조백신 확보에 성공하며 3상 투여가 가시화됐지만 국내에서는 아직 대조백신을 확보하지 못한 상태다. 하지만 GBP510이 국내 대조백신으로 적극 활용된다면 이 같은 어려움은 다소 덜어질 것으로 보인다.
한편 백신 개발을 포기한 곳도 있다. 제넥신 은 지난달 인도네시아에서 임상2·3상까지 승인받은 백신 후보물질 ‘GX-19N’의 임상을 철회했다. 코로나19 유행 상황과 백신시장 수급 상황 등을 봤을 때 개발에 따른 사업성이 낮다고 본 데 따른 것이다.
이춘희 기자 spring@asiae.co.kr
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>