口服混悬液已提交NDA申请…处方覆盖面扩大
Xcopri在美国年度销售额同比增长43.7%
Azetucalner正准备向FDA提交上市申请…竞争加剧成变量
在比利时全球制药企业UCB的Briviact物质专利于今年2月到期、导致癫痫治疗药物市场格局动荡之际,SK Biopharm的动向备受关注。SK Biopharm正以塞诺巴美特(美国商品名Xcopri)口服混悬液剂型为突破口,瞄准市场空隙。公司计划将原本难以通过片剂剂型覆盖的患者群体纳入处方范围,迅速填补市场空白。
据制药与生物行业8日消息,SK Biopharm近期已就塞诺巴美特口服混悬液剂型向美国食品药品监督管理局(FDA)提交了新药上市许可申请(NDA)。继原有片剂剂型之后,公司正推进追加剂型的审批,适应症为成人部分性发作(POS)患者。口服混悬液可提升难以吞咽片剂患者的用药便利性,并能灵活调整给药剂量,从而吸纳此前难以通过片剂触达的患者群体。根据去年在美国癫痫学会(AES)上公布的药代动力学(PK)研究结果,片剂与口服混悬液在体内吸收及药物暴露模式方面相似,已证明二者在药代动力学上具有等效性。
这一策略也与儿童临床试验相衔接。SK Biopharm目前正在开展儿童人群临床试验,并计划以本次NDA和儿童临床结果为基础,将给药年龄层依次扩展至儿童和青少年。SK Biopharm相关负责人表示:“我们将从以患者为中心的视角扩展治疗选择,解决多种患者群体尚未被满足的医疗需求,从而持续扩大处方基础。”
SK Biopharm之所以采取进取策略,背后是市场格局的变化。Briviact是美国癫痫治疗药物市场份额第一的药品,过去一直与Xcopri一起在新药序列中瓜分第3~4线处方位置。但随着专利到期,Briviact仿制药上市,含相同成分的Briviact被挤压至第1~2线处方阶段,而第3~4线新药处方位置则形成由Xcopri独占的格局。在美国,由于保险公司管理体系的原因,开具癫痫治疗药物时通常先使用仿制药,若疗效不佳才转用新药,这种分阶段处方结构已成惯例。业内分析认为,Xcopri在美国的物质专利将维持至2032年,有望在与竞争药物的较量中长期掌握市场主导权。
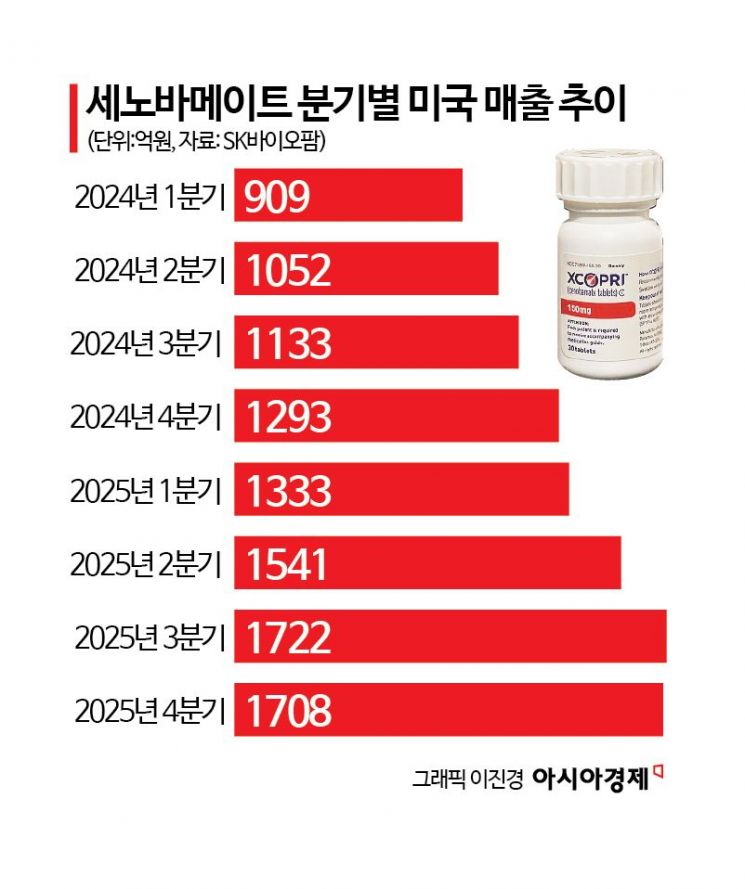
塞诺巴美特已步入高速增长轨道。在占全球癫痫治疗药物市场约70%的美国,Xcopri季度销售额从2024年一季度的6840万美元(约合909亿韩元)起步,飙升至2025年三季度的1.24亿美元(约合1722亿韩元)。去年美国全年销售额为4.432亿美元(约合6303亿韩元),较前年(3.216亿美元,约合4387亿韩元)同比增长43.7%。尽管受季节性因素和运输中库存影响,四季度销售额仅与前一季度持平,为1.179亿美元(约合1708亿韩元),但处方数量在去年12月达到4万7103张,创历史新高,意味着基础需求十分稳固。这一增长的根基在于其相较竞争药物具有明显的疗效优势。SK Biopharm方面表示:“截至目前,完全发作消失率超过20%的药物中,Xcopri是唯一的一款。”所谓完全发作消失,是指在药物给药期间完全没有出现发作,是衡量癫痫治疗药物的核心评价指标。
Kyobo证券研究员Jung Heeryeong表示:“随着排名第一药物Briviact在2月专利到期,以及适应症(PGTC)和儿童年龄段扩展带来的份额提升,有望实现占有率的扩大”,“从2026年的市场份额来看,有可能取得大幅提升。”不过,Xenon Pharmaceuticals的阿泽图卡尔纳(XEN1101)已公布三期临床主要结果,并正准备于今年下半年向FDA提交上市许可申请,未来竞争加剧的可能性仍是一大变量。三星证券研究员Seo Geunhee则表示:“在潜在竞争者Xenon Pharmaceuticals的XEN1101真正进入市场之前,已掌握真实世界证据(RWE)和营销基础设施的Xcopri,其寡头格局和随之而来的高增长态势不会受到破坏。”
版权所有 © 阿视亚经济 (www.asiae.co.kr)。 未经许可不得转载。