延世大学 Noh Jaeseok 教授团队:通过 METTL3-HNF1B 调控轴揭示胰腺癌治疗薄弱环节
癌细胞之所以能够在极端氧化应激环境中存活,其分子层面的原因被发现隐藏在附着于核糖核酸(RNA)上的“一种微小化学标记”之中。Yonsei University 生物化学系教授 Noh Jaeseok 研究团队阐明,RNA 修饰(m6A)可以调节维持癌细胞抗氧化防御体系的关键转录因子,并据此提出了全新的抗癌策略线索。
Noh Jaeseok 教授团队在国际学术期刊《核酸研究(Nucleic Acids Research)》上发表研究结果,指出结合于 RNA 的 m6A(N6-甲基腺苷)修饰通过维持转录因子 HNF1B 的表达,使癌细胞得以进行氧化应激防御并存活。
胰腺癌是在诊断后平均生存期极短、对治疗药物快速产生耐药且频繁复发、预后极差的典型难治性癌症。近期研究注意到,胰腺癌细胞通过代谢重编程和强大的抗氧化系统,即使在高度氧化应激条件下也能存活。因此,针对癌细胞特有的氧化还原(redox)调控机制,将其作为新的治疗靶点的尝试不断涌现。
瞄准的不是转录因子,而是“RNA 阶段”
转录因子是同时调控众多基因表达的关键蛋白,但从结构上看,并不存在可供药物结合的明确靶点位点,因此难以被直接靶向。研究团队为突破这一局限,没有直接针对转录因子本身,而是将目光投向生成转录因子的 RNA 阶段。
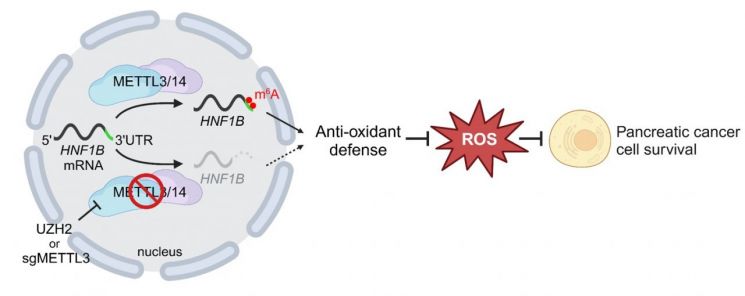
研究结果显示,由 METTL3-METTL14 组成的 RNA 甲基转移酶复合体在 HNF1B 信使 RNA(mRNA)的 3′ 非翻译区(3′-UTR)形成 m6A 修饰,而这一标记对维持 HNF1B 表达的稳定性和功能至关重要。也就是说,附着在 RNA 上的微小化学标记支撑着转录因子 HNF1B 的存在。
m6A 降低后,抗氧化防御崩溃
研究团队通过敲除或抑制 METTL3 基因功能,分析了降低 m6A 修饰时出现的变化。结果发现,由 HNF1B 调控的谷胱甘肽代谢显著减弱,癌细胞的抗氧化能力急剧下降。
还原型谷胱甘肽(GSH)减少,氧化型谷胱甘肽(GSSG)增加,导致细胞内氧化—还原平衡被打破,活性氧大量积累,使癌细胞对氧化应激变得极度脆弱。这一系列变化大幅提高了细胞走向凋亡的可能性。
研究团队还确认,当直接抑制 HNF1B 功能时,也会诱导出与 m6A 降低相似的氧化应激增加和细胞凋亡现象。该现象不仅在胰腺癌中出现,在多种癌种的细胞中也被普遍观察到,提示 HNF1B 很可能是调控整体癌症抗氧化防御的关键转录因子。
动物模型中同样证实肿瘤生长受抑
在动物模型实验中,METTL3 或 HNF1B 功能受抑制的肿瘤,其生长速度减慢,氧化损伤指标呈上升趋势。这一结果进一步佐证了 METTL3–HNF1B 调控轴在体内同样对肿瘤的生长和存活发挥重要作用。
本研究提出了一种连接结构:即作为“后转录组(epitranscriptomic)”信息的 RNA 修饰可以调控转录因子的表达和功能,从而维持癌细胞的代谢稳态与生存策略。研究团队将 METTL3–HNF1B 轴界定为癌症的一种新的“代谢脆弱点(metabolic vulnerability)”,并提出利用 m6A 调控机制开发下一代抗癌治疗策略的可能性。
Noh Jaeseok 教授表示:“本研究在分子层面展示了附着在 RNA 上的微小化学标记如何支撑癌细胞的生存策略”,并称“有望拓展为摧毁癌细胞所依赖的氧化应激防御体系的一种全新治疗路径”。
研究结果已于本月 6 日以“由 HNF1B 主导的氧化还原稳态受 RNA m6A 甲基化的系统性调控(Systemic control of HNF1B-driven redox homeostasis by N6-adenosine methylation)”为题在线发表。
本研究由 Yonsei University 生物化学系硕博连读研究生 Park Minji 作为第一作者参与,在韩国研究财团中坚研究者支援项目、Yuhan Corporation YIP 项目以及 BK21 项目的资助下完成。
版权所有 © 阿视亚经济 (www.asiae.co.kr)。 未经许可不得转载。

![“有钱也享受不到”……真正“顶级0.1%”的世界 [奢华世界]](https://cwcontent.asiae.co.kr/asiaresize/93/2026051507261063923_1778797570.png)







