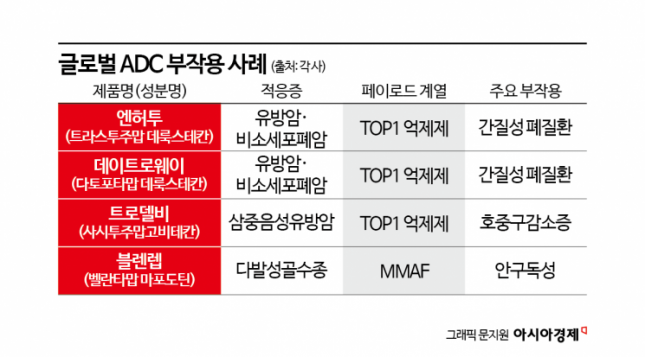
选择TOP1抑制剂的ADC,毒性副作用持续被报告
通过有效载荷多元化和连接子技术比拼安全性
一直被视为新一代抗癌药而备受关注的抗体-药物偶联物(ADC)接连陷入毒性副作用争议。国内主要企业处于临床阶段的ADC候选物质也采用了被全球学界指出存在毒性风险的有效载荷,负担正不断加重。
根据7日发表在国际学术期刊《柳叶刀·区域健康·欧洲》上的一项国际联合研究结果,ADC抗癌药在肺、肝、眼等部位出现的副作用持续被报告。尤其是肺毒性被列为可能导致患者死亡的严重不良反应。研究团队表示,“较早上市的第一代ADC在最大剂量给药时,毒性发生率一度超过50%”。
ADC是一类将针对癌细胞表面特异蛋白的抗体与强效毒性物质(有效载荷)结合的抗癌药物。当抗体与癌细胞结合后,有效载荷释放,从而杀死癌细胞。此时如果有效载荷在血液中提前释放,或附着在正常细胞上,就会引发毒性副作用。
这类毒性副作用同样出现在跨国制药巨头开发的治疗药物中。广泛用于治疗乳腺癌和非小细胞肺癌的Enhertu(成分名Trastuzumab Deruxtecan)就是代表性案例。由Daiichi Sankyo和AstraZeneca联合开发的Enhertu,去年在全球创下约5万亿韩元销售额,成为重磅ADC产品,但临床试验结果显示,约15%的给药患者报告出现间质性肺疾病。上市后开展的研究中,也有9.6%的患者被确认出现同样的不良反应。学界已将肺毒性明确列为Enhertu的“已确认风险(identified risk)”,并建议在治疗过程中进行密切监测。
导致毒性副作用的核心原因被指向特定有效载荷的“扎堆”现象。分析认为,众多企业集中采用“拓扑异构酶I(TOP1)抑制剂”类有效载荷,正在累积整体毒性风险。根据国际学术期刊《Nature Cancer》的报道,2024年进入临床阶段的ADC中,约60%采用了TOP1抑制剂类有效载荷。
TOP1抑制剂是一类阻断癌细胞分裂所需酶——拓扑异构酶I的毒性药物,其原理是阻碍DNA正常复制,从而杀死癌细胞。与其他有效载荷相比,该类药物药效略弱一些,但可以在单个抗体上结合更多分子,因此在提高效能的同时兼顾安全性,具有优势。自Enhertu采用TOP1抑制剂有效载荷并在全球市场取得成功后,后发企业纷纷选择同一类药物。
国内主要企业正在进行临床试验的多款ADC候选物质也大多选择了TOP1抑制剂类有效载荷。包括Celltrion的非小细胞肺癌治疗候选药物CT-P70在内,CT-P71、CT-P73等候选物全部以TOP1抑制剂类有效载荷“PBX-7016”为基础进行开发。ABL Bio通过其美国子公司Neok Bio开展临床试验的候选物ABL206和ABL209同样采用TOP1抑制剂类有效载荷。
随着ADC市场的评价标准从“疗效优先”转向“安全性优先”,国内ADC专业企业正推出绕开毒性瓶颈的差异化战略。
ABL Bio代表Lee Sanghun上月在美国癌症研究学会(AACR)上表示:“ABL206和ABL209将是最后的TOP1策略,此后管线将转向以双重有效载荷为中心。”双重有效载荷是指在一株抗体上同时搭载两种不同作用机制的药物,以摆脱对单一有效载荷的依赖,被视为新一代ADC的设计思路。
Ligachem Bio则将有效载荷分散至MMAE、MMAF、PBD等多个类别,以降低对单一有效载荷的依赖风险。向美国Johnson & Johnson完成技术转让的核心候选物LCB84没有采用TOP1抑制剂,而是选择了MMAE类有效载荷。公司方面称,其应用了连接抗体与有效载荷的连接子(linker)技术“ConjuAll”,设计思路是使有效载荷不在血液中泄漏,只在肿瘤细胞内部释放。
IntoCell则通过直接改造有效载荷本身,开发降低正常细胞摄取的有效载荷改造技术(PMT)。其方式是对有效载荷进行化学处理,使其不易附着正常细胞,从而减少副作用。首个临床候选物ITC-6146RO在采用比TOP1抑制剂药效更强的Duocarmycin的同时,通过PMT技术降低了对正常细胞的渗透风险。如果说Ligachem Bio是在连接子层面提升安全性,那么IntoCell则是通过改造有效载荷本身来实现差异化。
版权所有 © 阿视亚经济 (www.asiae.co.kr)。 未经许可不得转载。