(后排自左起)化学系研究教授 Lee Hoyeon、硕士研究生 Lee Gyuhan、博士研究生 Park Junhyeok、博士研究生 Park Yeo Jin,(前排自左起)硕博连读研究生 Park Hyeongbin(第一作者)、教授 Kim Mingon(通讯作者)、硕士研究生 Yoon Jiyoung。GIST提供
View original image光州科学技术院(GIST)30日表示,化学系 Kim Mingon 教授研究团队提出了一项能够灵活设计并检测多种疾病靶标基因的下一代基因诊断技术。
该技术可以针对需要诊断的“靶标基因”设计定制化诊断方法,因此可应用于传染病、癌症、遗传病等多种疾病的诊断。
基于人体或病毒所含遗传信息(DNA或RNA)来诊断疾病的基因诊断技术,已广泛用于多种疾病诊断。目前作为标准诊断方法使用的基因扩增检测(聚合酶链式反应,Polymerase Chain Reaction,PCR)虽然具有较高的准确度和灵敏度,但存在耗时较长、需要专业设备和人力等局限。
为弥补这一局限,将针对与疾病相关的特定基因的“基因剪刀(CRISPR)”与在恒定温度下快速大量复制基因的“等温扩增技术(Isothermal amplification)”相结合的“单管反应诊断法(One-pot CRISPR)”正受到关注。
然而,这些技术在寻找基因并发出信号的反应速度不同,且难以调控,因此难以针对每个基因找到最优条件,设计的灵活性也受到限制。
为解决这一局限,研究团队提出了一种通过调控基因剪刀技术,能够通用性检测用于判断疾病有无的“靶标基因”的新方法。在基因剪刀技术中,类似于汽车中导航仪角色的向导(RNA,核糖核酸)找到靶标基因后,真正起作用的发动机(负责切割基因的Cas蛋白)会在该基因部位切割基因并产生信号。
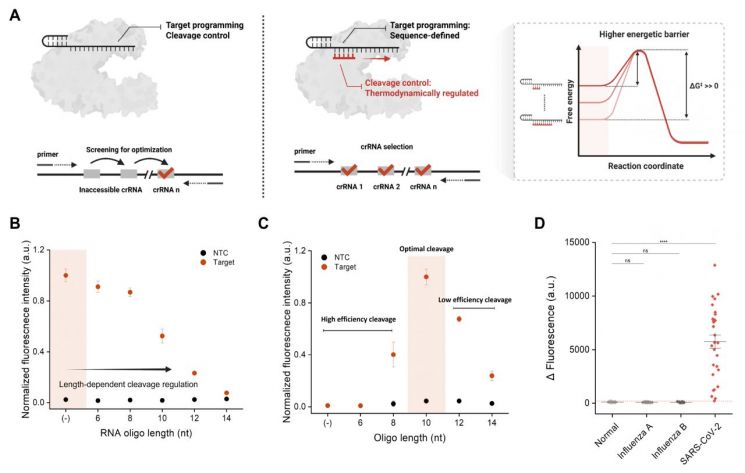
研究团队在此基础上,引入了长度较短、发挥类似刹车作用的“基因片段(寡核苷酸·oligo)”,从而能够独立调控切割基因并发出信号这一过程的速度。
研究团队利用基因模型,采用不同长度寡核苷酸进行实验,确认到反应速度会像刹车力度随寡核苷酸长度变化而精细调节,并据此提出了可用于设计最优条件的规律。此外,将实验结果应用于从实际患者采集的120份检体时,能够在约20分钟内判读感染与否,并表现出与定量PCR(基因扩增检测)相似水平的准确度和灵敏度,从而证实在较既有方法更快速的同时,也能够实现高可靠性的诊断,并验证了其临床应用可能性。
该技术不局限于某一特定疾病,而是可以通用性地应用于多种基因靶标。通过调控寡核苷酸的设计,可应用于从新冠肺炎等传染病到各类癌症诊断等多个领域,并能以一个平台诊断多种疾病。此外,无需像以往那样针对每个基因反复优化条件,可简化疾病诊断设计,大幅提升开发效率。
Kim Mingon 教授表示:“本研究的意义在于,这不是针对单一特定疾病的技术,而是展示了可根据多种基因靶标进行设计的诊断平台的可能性。当前我们主要围绕来源于实际传染病患者的样本验证了性能,今后有望扩展应用到癌症、遗传性疾病等多个领域。”
此次研究由GIST化学系 Kim Mingon 教授指导,硕博连读研究生(第一作者) Park Hyeongbin 参与完成,得到了科学技术信息通信部和韩国研究财团全球研究网络项目及先导研究中心支持项目(IRC),以及国家科学技术研究会(NST)融合研究团项目的资助。研究结果已于2026年3月3日在线发表在生物化学及分子生物学领域权威国际学术期刊《Nucleic Acids Research》上。
版权所有 © 阿视亚经济 (www.asiae.co.kr)。 未经许可不得转载。