结合人工智能、计算模型与神经科学,揭示运动协同发育原理
有望用于帕金森等运动障碍研究以及机器人和物理人工智能应用
研究证实,人类在行走或奔跑时表现出的精细运动协同能力,其核心机制源自小脑中的一种非神经元细胞——“星形胶质细胞(astrocyte)”。该研究突破了以往认为脑发育过程仅围绕神经元展开的传统观点,提出了一个新的脑发育概念:神经元与胶质细胞之间的协作结构共同推动运动功能的成熟。
基础科学研究院(IBS)记忆及胶质细胞研究团认知及胶质细胞科学组组长 Lee Changjun 和研究委员 Hong Seongho 领导的研究团队于9日表示,他们揭示了小脑星形胶质细胞调控神经回路、从而实现复杂而精细运动的机制。
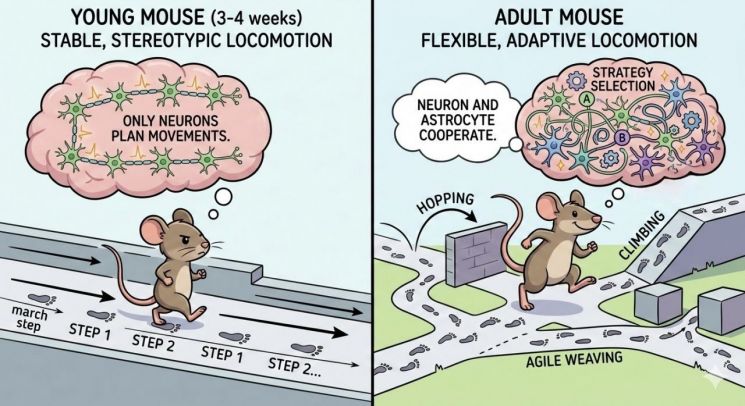
随生长而发生的小脑回路变化及其导致的运动协同差异示意图。幼年小鼠个体中,由神经元核心回路产生的抑制信号占主导作用,因而仅表现出重复且受限的步行模式。相反,在成体中,星形细胞也参与抑制信号的调节,使机体能够灵活组合多种动作,实现多样化的运动协同。研究团队提供
View original image小脑抑制信号的变化……星形胶质细胞主导调控
小脑中汇集了全脑70%以上的神经元细胞,其中大部分为颗粒细胞(cerebellar granule cell)。这些细胞通过由神经递质γ-氨基丁酸(GABA)介导的“持续性抑制(tonic inhibition)”来调节其活性。研究团队关注到,个体发育过程中这种抑制信号的调节方式可能会发生改变。
实验结果显示,在幼年小鼠中,由抑制性神经元释放的GABA承担了持续性抑制的功能。然而在成体阶段,星形胶质细胞通过名为“Bestrophin-1”的离子通道直接提供GABA,并在抑制调控中发挥核心作用。也就是说,在发育过程中,小脑回路从“以神经元为中心的调控体系”转变为“由神经元与星形胶质细胞共同调控的体系”。
小脑运动协同的关键……通过人工智能行为分析加以验证
为分析这一变化对神经回路功能的影响,研究团队构建了一个包含约100万枚神经元的大规模小脑神经回路计算模型。仿真结果表明,随着抑制调控的中心逐渐转移至星形胶质细胞,颗粒细胞之间的相互干扰减少,从而可以更加独立地处理不同的运动信息。
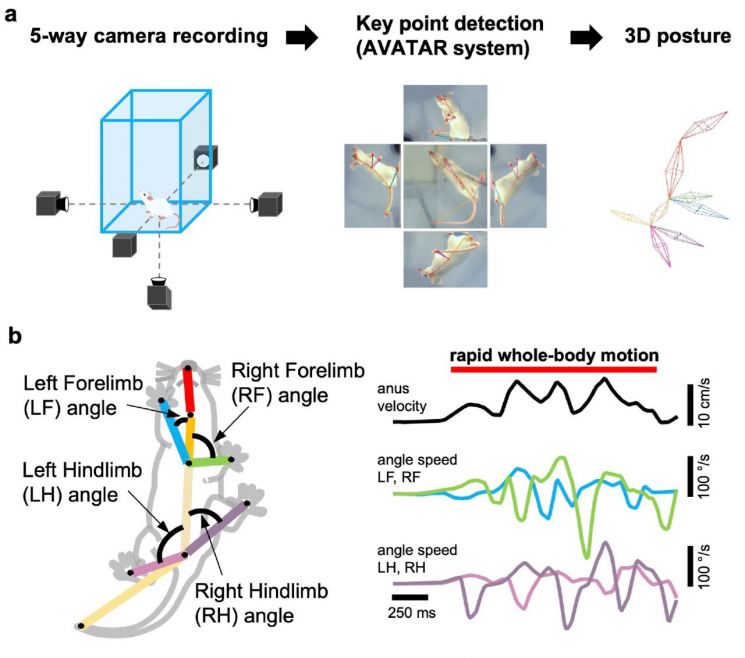
基于人工智能的三维行为分析验证星形胶质细胞来源GABA的运动协调功能。(a) 利用5台从多角度拍摄的摄像机获取的视频,通过人工智能分析系统AVATAR进行处理,提取小鼠身体主要部位的坐标,并据此重建三维骨骼运动。(b) 对重建的三维骨骼数据进行分析发现,在成体中缺失星形胶质细胞来源GABA时,四肢运动的独立性下降,运动协调能力随之减弱。研究团队提供
View original image此外,研究团队利用基于深度学习的三维行为分析系统“AVATAR 3D”对小鼠的运动进行了精细分析。结果发现,在正常成体小鼠中,可以观察到由四肢动作彼此独立组合而成的多种运动模式。相反,在幼年小鼠或Bestrophin-1基因缺失的成体小鼠中,运动形式的多样性大幅下降。
研究团队表示,通过这些结果,他们不仅在细胞层面,而且在实际行为变化层面证实,小脑星形胶质细胞是运动协同能力成熟的关键调节者。
IBS记忆及胶质细胞研究团团长 Lee Changjun 表示:“本研究成果显示,在脑发育过程中,不仅神经元本身重要,与星形胶质细胞之间的相互作用同样发挥关键作用。预计这一发现不仅可用于发育性和退行性运动障碍的研究,还将有助于基于脑原理的机器人与物理人工智能运动控制技术的开发。”
本研究成果已于上月18日在线发表在国际学术期刊《Experimental & Molecular Medicine》(《实验与分子医学》)上。
版权所有 © 阿视亚经济 (www.asiae.co.kr)。 未经许可不得转载。








