被认为是阿尔茨海默型痴呆主要致病原因之一的Tau蛋白在大脑中如何发生聚集和纤维化,其分子水平机制已由国内研究团队首次在全球范围内加以证明。
韩国保健产业振兴院4日表示,由首尔大学医学院医科科学系教授 Lee Minjae 等多学科研究团队与高丽大学化学系教授 Kim Jungon 研究团队合作,首次证明了Tau蛋白的纤维化过程及其形成神经毒性物质的原理。
据悉,在痴呆患者中占70%至80%的阿尔茨海默型痴呆,是由淀粉样蛋白β(Aβ)和Tau等蛋白在大脑中堆积,形成杀死神经细胞的毒性物质,被视为主要发病机制。然而,这些蛋白为何会堆积等更为根本性的发病机理尚未被揭示,一直成为开发根本性治疗药物(疾病修饰治疗药物,DMT)的障碍。
据介绍,本次研究具体阐明了迄今尚未被揭示的Tau蛋白纤维化现象,包括Tau蛋白片段渗入脑神经细胞内部的过程、抑制突触功能的机制、对动物记忆力减退及脑组织坏死的影响等。
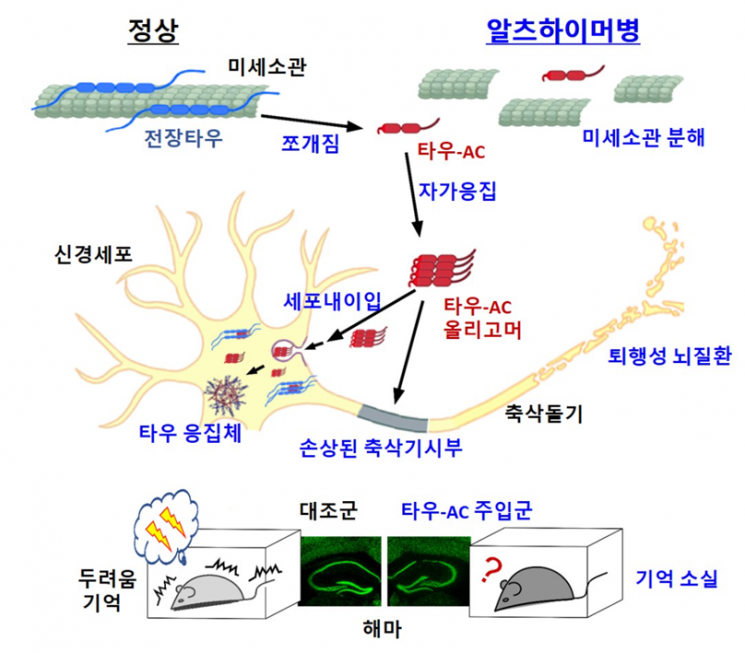
研究团队为弄清Tau蛋白在分子水平上如何发生纤维化,将研究重点放在促进神经毒性物质形成的关键区域(聚集核心)上。结果发现,内部被切割的Tau蛋白部分片段在无需额外处理的生理环境条件下即可自发形成神经毒性物质,并具有将正常Tau蛋白也转化为神经毒性物质的能力。研究还确认,其原因在于蛋白质被切割后,导致特定部位(聚集核心,Tau-AC)暴露。
此外,研究团队还阐明了由Tau切割产生的神经毒性物质渗入神经细胞的路径、诱导进一步聚集的过程,以及降低神经细胞突触可塑性的现象,从而在细胞水平上确立了这些物质诱发病理变化的机制。
在动物模型实验中,研究团队将Tau聚集核心注入小鼠脑室内的海马体后,观察到神经细胞死亡、神经炎症反应以及记忆力减退等与阿尔茨海默型痴呆相似的行为学变化,由此确认了在分子与细胞水平上阐明的Tau片段病理机制在动物模型中同样可以再现。
主导该研究的 Lee Minjae 教授表示:“本研究在分子、细胞以及动物模型层面揭示了Tau蛋白新的纤维化及神经毒性生成原理”,并称“通过后续研究,有望为提出阿尔茨海默病新的治疗方法作出贡献”,从而说明了研究的意义。他接着强调:“通过生物化学、神经科学、生物物理学等多个领域研究者的协作,以及国家对高风险、高回报基础研究的支持,才得以产出此次研究成果”,并指出政府有必要持续支持富有创意的研究与开发(Research and Development,R&D)活动。
本项研究在痴呆克服研究开发事业团的支持下完成,并于上月18日在线发表在国际学术期刊《Advanced Science》上。
版权所有 © 阿视亚经济 (www.asiae.co.kr)。 未经许可不得转载。

![100万亿恐打水漂…“三星罢工成史上级利好” 价格暴涨20%市况大乱 [台湾芯片通信]](https://cwcontent.asiae.co.kr/asiaresize/93/2026051416263163580_1778743590.jpg)







