在原因不明的情况下肺部逐渐变硬的“特发性肺纤维化”的恶化机制,已被国内研究团队揭示。
疾病管理厅国立保健研究院28日表示,在特发性肺纤维化的进展过程中,研究团队阐明了调节免疫异常反应的“ATF3(Activating Transcription Factor 3)”基因的新功能。
国内研究团队阐明调节免疫异常反应的“ATF3”基因
ATF3是指当细胞受到炎症或各种应激刺激时被激活,用于调节体内代谢作用和免疫反应的活性转录调节因子。
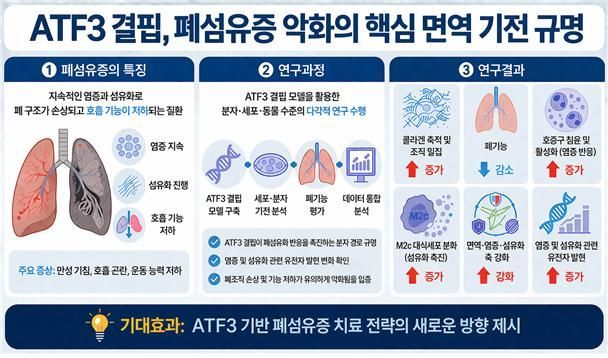
特发性肺纤维化是一种病因不明确的难治性肺部疾病,肺组织逐渐变硬,导致呼吸功能下降。随着病情进展,患者会出现气促,日常生活受到严重影响,且通常在确诊后数年内死亡,预后极差。
目前已开发并使用“吡非尼酮(pirfenidone)”和“尼达尼布(nintedanib)”两种治疗药物,但只能延缓疾病进展,尚无法实现治愈。为此,国立保健研究院一直在开展研究,以阐明肺纤维化的发生机制,并找出能够调控纤维化进程的重要因子及其作用机制。
研究团队为确认在炎症或应激刺激时早期被激活、广为人知的转录调节因子ATF3,究竟如何在实际肺脏中调节免疫机制和肺纤维化,利用缺失ATF3的实验动物模型诱导肺纤维化。
结果显示,在缺乏ATF3的情况下,肺功能下降更为明显。与正常组(约减少15%~20%)相比,缺乏ATF3的实验组肺容量减少20%~25%,肺弹性增加、肺顺应性下降,呈现出肺部更加僵硬的状态。这表明,ATF3缺失会加速肺纤维化进程并加重肺功能受损。
ATF3缺失还会显著增强肺组织内的炎症反应。负责炎症早期反应的中性粒细胞增加约10倍,促进纤维化的M2c表型巨噬细胞也增加6.5倍,免疫细胞构成出现异常变化。同时,与纤维化相关的基因表达也有所增加,炎症与组织损伤同步被强化。
缺失时肺容量最多减少25%……提示治疗新可能
在转录组分析中,ATF3缺失组的炎症及纤维化相关基因表达增加1.5倍以上,免疫和炎症相关通路被激活。这进一步印证了ATF3通过调节免疫反应,在抑制肺纤维化进程中发挥重要作用。
研究团队表示:“本研究阐明了在肺纤维化进展过程中,同时调节免疫细胞炎症反应和组织纤维化的新分子机制。具有对早期应激作出反应功能的ATF3基因,通过抑制炎症反应的过度激活,减轻肺纤维化进程,这一点具有重要意义。”
国立保健研究院慢性疾病融合研究部部长Kim Wonho表示:“肺纤维化是一种难以治疗的慢性肺部疾病,因此新的治疗策略至关重要。今后我们将继续阐明慢性呼吸系统疾病的发病机制,并推进可实际应用于患者治疗策略的相关研究。”
本研究成果已于今年2月发表在过敏与免疫科学领域顶级国际学术期刊《Clinical Science》上。






![[现场报道]“说了只会吵架”……戒严后更加隐匿的忠南真实民意](https://cwcontent.asiae.co.kr/asiaresize/304/2026051223490460082_1778597344.jpg)
