由盈转亏的三日制药,CDMO 延迟叠加主力品种流失陷入“双重困境”
by Lee Sungmin
Published 06 Feb.2026 08:59(KST)
越南 CMO 工厂全球 GMP 认证延迟
“上半年获得 KGMP 后商业化生产将全面展开”
三日制药 (삼일제약) 的盈利能力亮起了警报灯。曾经每年实现约 100亿韩元销售额的核心品种“Gliptide片 (글립타이드정)”事实上进入处方流失阶段。在越南的滴眼液委托开发生产(CDMO)项目也因认证延迟而无法启动商业化生产的情况下,市场对其短期业绩防御能力的担忧正在加剧。
据业内 6日消息,食品医药品安全处前一日根据药品安全性和有效性再评价结果,向医师、药师及患者发放了信息函,针对Sulglikotide 制剂建议停止使用并改用替代药品。监管部门认为,虽然安全性不存在问题,但未能证明其在治疗胃、十二指肠溃疡及胃、十二指肠炎方面的疗效。
三日制药是国内唯一拥有 Sulglikotide 制剂 Gliptide片的企业。Gliptide片在三日制药整体销售额中占比约 5%,年销售规模约为 100亿韩元。继 Livact(肝硬化患者用营养剂)、Foributin(胃肠运动调节剂)、Monoprost(青光眼滴眼液)之后,是三日制药内部屈指可数的主力产品。
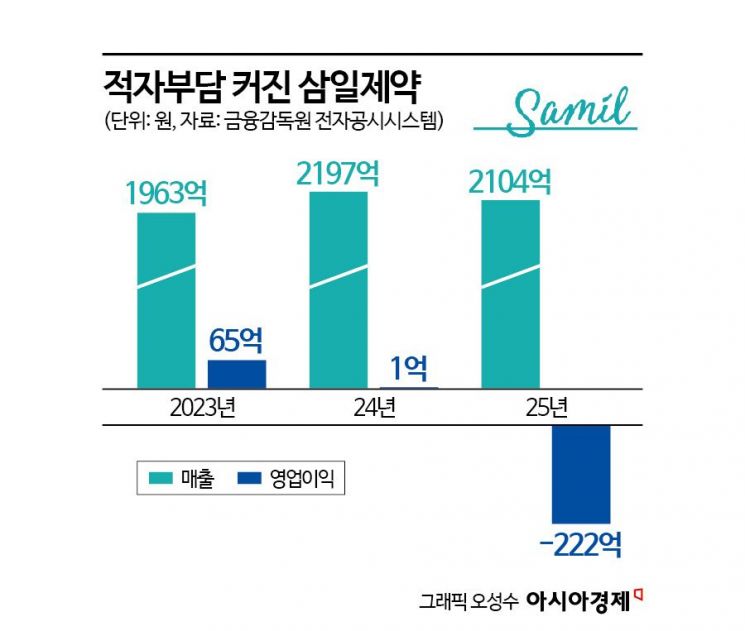
问题在于,这一利空与业绩不振局面叠加出现。三日制药去年按合并基准实现销售额 2104亿韩元,营业亏损 222亿韩元,转为亏损。销售额较前一年减少 4.2%。公司将主要产品销售下滑、技术开发费用增加,以及越南法人为商业化生产做准备和通过药品生产及质量管理基准(GMP)认证过程中销售与管理费用上升,列为业绩恶化的原因。
三日制药向越南滴眼液 CDMO 项目投入约 1300亿韩元,但尚未转化为销售,这一点被视为一大负担。公司于 2018 年在越南设立法人,此后在 2022 年建成一座年产约 3亿支滴眼液规模的 CDMO 工厂。但业内评价认为,为全面投产所需的认证程序延迟,导致商业化生产转型进度放缓。
全球委托生产(CMO)和 CDMO 业务要实现客户订单和商业化生产,必须取得药品生产及质量管理基准(GMP)认证。三日制药尚未完成全部主要认证程序。公司在 2024 年取得越南 GMP 认证,但此后计划争取的韩国 KGMP 认证程序出现延误。美国食品药品监督管理局(FDA)的现行药品生产质量管理规范(cGMP)认证和欧洲 EU-GMP 认证也尚未到手。公司方面表示,如果今年获得 KGMP 认证,商业化生产有望逐步扩大。
业界评价认为,在既有产品销售增长停滞的背景下,三日制药能否恢复盈利,最终取决于今年在取得 GMP 认证之后,CDMO 商业化生产能否真正转化为销售收入。三日制药相关负责人表示:“全球 CMO、CDMO 药品业务的关键在于高品质和成本竞争力”,并称“公司将以越南较低的人力成本为基础,确保成本竞争力,同时凭借在眼科药品生产方面的经验维持品质竞争力,把该业务培育为中长期增长动力”。