[电池完全征服]⑧连文科生都看得懂的氧化与还原
by Kang Heejong
Published 21 Oct.2023 08:00(KST)
电池是如何“装进”电能又将其释放出来的呢?电池的基本原理,是把化学能转化为电能。人们往往以为电池是在储存能量或电力,但实际上,是通过电池内部发生的化学反应来产生电能。从1800年意大利科学家Alessandro Volta发明的所谓“伏打电池”起,到如今广泛应用于电动汽车的锂离子电池,原理都是相同的,只是根据在电池中选用和组合何种物质不同,性能有所差异而已。直到现在,众多科学家仍在日夜研究,试图找到既性能优异又安全可靠的电池材料最佳组合。
氧化与还原:失去与获得电子
要理解电池的原理,首先要明白氧化(Oxidation)和还原(Reduction)的概念。将物质一再分割,最终会得到原子。原子由原子核和绕核运动的电子构成。在满足一定条件时,电子会从原子中脱离并自由移动,这种电子称为自由电子。电池中所谓有电流流动(产生电流),就是构成正极和负极的物质之间发生电子自由移动的现象。用来解释这种电子移动的,就是氧化和还原过程。
从经典意义上说,某种物质得到氧(氧化)或失去氧(还原),就是氧化与还原。此后,这一概念又扩展为失去氢(氧化)和得到氢(还原)。再广义一些,就把失去电子称为氧化,得到电子称为还原。也可以用“氧化数”这一用数值表示电子得失多少的概念来解释氧化和还原:氧化数增加为氧化,减少为还原。
在化学键的形成与断裂过程中,氧化与还原总是同时发生,统称为氧化–还原(redox)反应。将金属铜浸入硝酸银溶液中,溶液颜色会变为蓝绿色,同时有金属银析出(在液体中生成固体)。铜把2个电子给了硝酸银溶液中的银离子,自身变成铜离子进入溶液(氧化);硝酸银溶液中的银离子接受2个电子,变成金属银(还原)。用化学方程式可表示如下。
铜与氧反应生成氧化铜(2CuO)时,铜放出2个电子而被氧化,氧从铜那里得到2个电子而被还原。自身被还原、使其他物质被氧化的物质称为还原剂;相反,自身被氧化、使其他物质被还原的物质称为氧化剂。在氧化铜中,氧是氧化剂,铜是还原剂。
电池正是由这样的氧化和还原过程构成的。电池大致由正极(cathode)和负极(anode)组成,正极和负极统称为电极(electrode)。
在电池中,发生还原反应的地方定义为正极,发生氧化反应的地方定义为负极。电子从发生氧化反应的负极(失去电子的一侧)出发,经导线移动到发生还原反应的正极(得到电子的一侧)。
电流则被规定为反方向,从正极流向负极。电子移动方向与电流方向相反,是因为人类较晚才发现电子的移动。科学家在发现电现象时,就先定义电流是从正极流向负极,而后来才弄清电子实际上是从负极移动到正极。
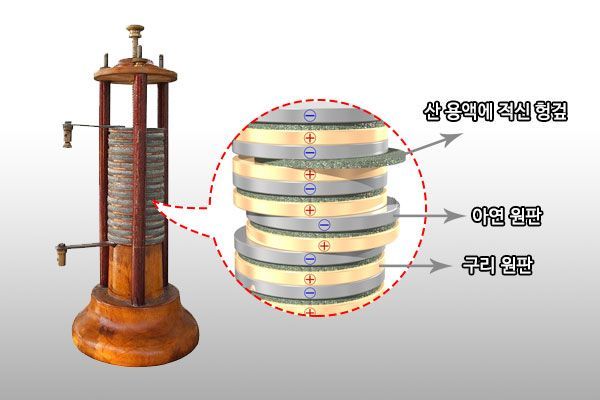
最早的化学电池——伏打电池,也可以用氧化和还原来解释。伏打电池是在稀硫酸溶液(H2SO4)中插入锌(Zn)金属板和铜(Cu)金属板,并用导线将两块金属板连接起来的结构。
此时,在锌金属上发生的是放出电子的氧化反应,在铜上发生的是接受电子的还原反应。从锌放出的电子沿导线向铜板方向移动,而电流则反向从铜流向锌。伏打电池中,这样的化学反应持续进行,从而不断有电流输出。
此时失去电子的锌变成锌离子(Zn2+),从金属板上脱离并溶解到硫酸溶液中。移动到正极的电子与溶液中溶解的氢离子(H+)结合,被还原为氢气(H2)。
用化学方程式表示如下。
在电池中,提供电子的物质称为负极活性物质(活性材料),获得电子的物质称为正极活性物质。在伏打电池中,锌是负极活性物质,氢离子是正极活性物质。同时,氢离子是氧化剂,锌是还原剂。
那么,为什么有的物质会被还原,有的物质会被氧化呢?决定氧化和还原的是电离倾向。也就是说,根据电离倾向的不同,在电池中可以成为负极,也可以成为正极。氧化倾向越强,就越适合作为负极材料;还原倾向越强,就越适合作为正极材料。
电离倾向,是指金属物质失去电子、变成阳离子的性质(易被氧化的性质)。科学家根据各种物质的反应性,计算出电离倾向并制成表格。中学和高中化学课上背过的那串顺口溜,说的就是这个顺序:“钾(K)>钙(Ca)>钠(Na)>镁(Mg)>铝(Al)>锌(Zn)>铁(Fe)>镍(Ni)>锡(Sn)>铅(Pb)>氢(H)>铜(Cu)>汞(Hg)>银(Ag)>铂(Pt)>金(Au)”,越靠前越容易被氧化。以氢为界,往左侧越走越容易被氧化,往右侧越走越容易被还原。
例如,在稀盐酸(2HCl)中放入锌(Zn),电离倾向比氢更大的锌会放出2个电子(氧化)。这些电子与盐酸中的氢离子(2H+)结合,被还原生成氢气(H2)。
离子,是指通过得到或失去电子而带有电荷(electric charge,电的性质)的原子或分子。失去电子的叫阳离子,得到电子的叫阴离子。我们之所以把锂离子电池与锂电池区分开来,是因为电池内部的锂不是以金属锂,而是以锂离子形式存在。
电压如何产生:标准还原电位
当电子在正极或负极处移动时,会产生电荷的势能,这就是电位(electric potential)。就像水位越高,往下落的力量越大一样,电位越高,意味着电子向另一方向移动的驱动力越大。电位取决于金属的反应性,也就是电离倾向。
科学家以标准状态下氢与氢离子之间产生的电位值为基准,求得其他金属的相对电位值,这就叫标准还原电位(Standard Reduction Potential)。所谓标准状态,是指温度25℃、压力1个标准大气压(1 atm)、离子浓度1摩尔(1 M)。电位的单位用伏特(V)表示。例如,锌的标准还原电位是-0.763 V,这意味着它比氢–氢离子之间产生的电位(0 V)低0.763 V。
标准还原电位为正值(+)时,表示在标准状态下比氢离子更容易被还原;为负值(-)时,则表示不易被还原。由于标准还原电位是以还原性为基准表示的,因此若要理解氧化性,只需反向来看:数值越负,越容易被氧化(越容易失去电子)。
锂的标准还原电位是-3.045。锂是一种极易被氧化的金属。正因为锂具有这样的性质,最初以金属锂作为负极的电池研究非常活跃。但后来,日本的Yoshino Akira博士采用John Goodenough教授开发的锂钴氧化物(LCO)作为正极材料,锂离子电池由此诞生。这也是他们在2019年共同获得诺贝尔化学奖的背景。
标准还原电位只测量电极的一半,因此也称为“半电位”(半电极电位)。当电位不同的物质相接触时,会产生电位差,这就是起电力(electromotive force)。从汉字字面理解,“起电力”就是“产生电的力量”,其原理与水从高处流向低处相同。起电力的单位同样用伏特(V)表示。在电池中,正极和负极之间的电位差就表现为起电力(电压)。
电池的起电力(E)大小,可用“正极的标准还原电位-负极的标准还原电位”来计算,这与在建筑物中用顶层楼层数减去地下楼层数来求总层数的公式类似。
在伏打电池中,氢离子(0 V)实际上起正极活性物质的作用,因此其起电力为0-(-0.763)=0.763 V。从理论上说,如果分别用电位差较大的金属作正极和负极材料,就可以获得较高电压。
伏打电池的起电力(E)=0-(-0.763)=0.763 V
伏打电池与丹尼尔电池
不过,尽管伏打电池在科学上具有重大意义,但由于会在正极铜板上产生氢气附着的“极化现象”,在实际使用上存在困难。对伏打电池加以改良,制造出世界上第一种实用化学电池的人,是英国化学家John Frederic Daniell。1836年,Daniell在盛有硫酸溶液的多孔陶罐中放入锌电极,再把这只陶罐浮置在装满硫酸铜溶液的铜制容器中,构成一种电池。陶罐上有微小孔洞,使得各自容器中产生的离子可以相互迁移。与伏打电池相比,丹尼尔电池更加稳定、寿命更长,成为现代一次电池的基础。丹尼尔电池的起电力为1.1 V。
![[电池完全征服]⑧连文科生都看得懂的氧化与还原](https://cphoto.asiae.co.kr/listimglink/1/2023102014202323055_1697779223.png)
![[电池完全征服]⑧连文科生都看得懂的氧化与还原](https://cphoto.asiae.co.kr/listimglink/1/2023102010232722728_1697765007.jpg)
![[电池完全征服]⑧连文科生都看得懂的氧化与还原](https://cphoto.asiae.co.kr/listimglink/1/2023102013253422977_1697775934.jpg)
![[电池完全征服]⑧连文科生都看得懂的氧化与还原](https://cphoto.asiae.co.kr/listimglink/1/2023102008045322308_1697756693.jpg)
![[电池完全征服]⑧连文科生都看得懂的氧化与还原](https://cphoto.asiae.co.kr/listimglink/1/2023102012514022949_1697773900.jpg)
![[电池完全征服]⑧连文科生都看得懂的氧化与还原](https://cphoto.asiae.co.kr/listimglink/1/2023102012435322947_1697773433.jpg)
![[电池完全征服]⑧连文科生都看得懂的氧化与还原](https://cphoto.asiae.co.kr/listimglink/1/2023102012543822952_1697774077.jpg)
![[电池完全征服]⑧连文科生都看得懂的氧化与还原](https://cphoto.asiae.co.kr/listimglink/1/2023102011331522912_1697769195.jpg)