UNIST Park Chanyoung教授团队发现与癌症发生相关的“Entosis”现象
Published 30 May.2023 09:05(KST)
Updated 07 Aug.2025 09:18(KST)
联合国科学技术院生命科学系教授 Park Chanyoung 研究团队近期发现了调控癌细胞新型细胞死亡的机制,为加深对癌发生过程的理解提供了新的线索。
正常细胞在营养不足、缺氧等压力环境下会通过细胞凋亡(apoptosis)而死亡。但癌细胞即便在压力环境中也能克服细胞凋亡,不断增殖,并逐步发展出有利于自身生存的机制。
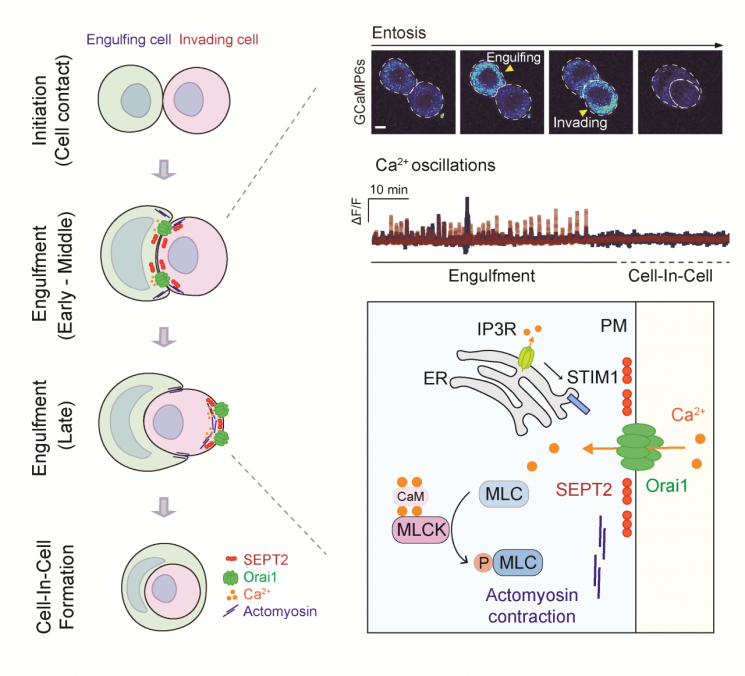
近来,在这一过程中发现了非凋亡性细胞死亡(non-apoptotic cell death),即吞噬性内陷(Entosis)。吞噬性内陷是一种细胞吞噬现象:存活的癌细胞(侵入细胞)侵入到另一颗癌细胞(吞噬细胞)内部,形成“细胞中有细胞”的结构。
癌细胞通过吞噬性内陷,为规避免于细胞死亡营造出有利环境。吞噬细胞从侵入细胞获得营养和染色体,而侵入细胞则躲藏在吞噬细胞内部,在合适时机逃出,或在吞噬细胞内进行分裂。
这种吞噬性内陷通过癌细胞相互作用引发的染色体数目异常等基因组不稳定性,影响癌症的发生和发展。因此,若要研究癌细胞导致癌症发生的原因及治疗方法,就必须深入理解吞噬性内陷。
据研究团队介绍,在癌症发生初期,自由移动的癌细胞(侵入癌细胞和吞噬癌细胞)会在细胞内部或细胞之间触发特殊的信号机制。
其中,钙通道依赖型蛋白质的信号传导也被认为是癌细胞信号传导以及癌细胞之间相互作用的关键机制之一,但其与吞噬性内陷之间的关联尚未得到研究。
研究团队在本次研究中证实,存在于细胞膜上的钙通道蛋白 Orai1 的信号传导机制,是诱导癌细胞发生吞噬性内陷所必需的。
他们观测到,在侵入癌细胞和吞噬癌细胞中,Orai1 在细胞骨架蛋白之一的隔膜蛋白(septin)的作用下,仅局部移动到细胞膜的特定区域,并在相同位置呈现出具有特征性的振荡(oscillation)模式,从而引发细胞内部局部浓度变化。
这一钙信号传导机制会使细胞运动所必需的动力蛋白肌球蛋白发生磷酸化,进而诱导细胞骨架重排或促使细胞发生运动。
研究团队据此阐明了吞噬性内陷被诱导并推进的具体机制。同时,他们还发现,只要调控 Orai1 通道或其信号传导机制,就能抑制吞噬性内陷,从而提出了有望调控依赖吞噬性内陷的癌发生过程的可能性。
生命科学系教授 Park Chanyoung 表示:“本研究揭示了在癌发生、转移以及癌细胞吞噬性内陷(细胞中有细胞现象)诱导机制中,Orai 钙通道所发挥的新型信号传导机制。今后,通过对钙通道信号传导调控以及吞噬性内陷调控的研究,有望为癌症发生、转移及治疗策略研究提供帮助。”
本研究在科学技术信息通信部和韩国研究财团的全球博士后奖学金项目、中坚研究者支援项目以及先导研究中心的资助下开展。研究成果已于3月24日在线发表在国际学术期刊《Advanced Science》上,并于5月17日正式出版。