식약처, 임상시험 발전 5개년 종합계획 발표
현행 일률적 심사서 위험도에 따른 심사키로
[아시아경제 조현의 기자] 앞으로 글로벌 임상시험 선점 경쟁이 치열해지면서 안전성이 확보된 임상시험은 필수정보만으로 승인하는 '차등승인제'가 단계적으로 도입된다. 임상시험 안전관리 강화 차원에서 임상시험 과정에서 발생하는 모든 안전성 정보에 대한 정기보고도 의무화된다.
식품의약품안전처는 8일 이 같은 내용을 담은 '임상시험 발전 5개년 종합계획'을 수립했다고 밝혔다.
이 계획은 크게 ▲임상시험 안전관리 체계 확립 ▲임상시험 국제 경쟁력 강화 ▲환자 치료 기회 확대 및 소통체계 구축 등 3개 추진과제로 나뉜다.
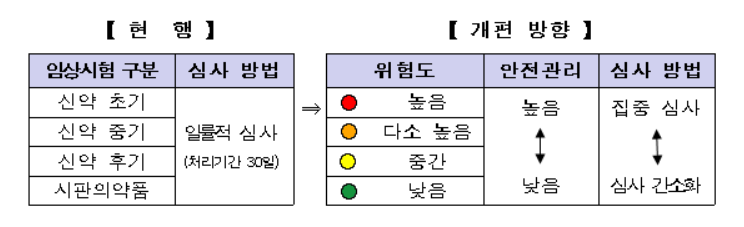
식약처는 우선 법 개정을 거쳐 2021년부터 임상 의약품의 위험도에 따라 심사를 간소화하거나 집중 심사하는 식으로 차등을 두는 차등승인제가 도입된다. 주요 국가에서 승인한 다국가 임상 3상시험 등 위험도가 낮은 임상시험부터 의약품 정보, 임상시험 실시기관, 임상시험심사위원회(IRB) 승인 여부 등 필수 정보만 있으면 승인해준다. 다만 안전조치로 IRB 심의요건을 강화하고 심의 결과 정기적 제출, 상시 모니터링 절차 등도 마련하기로 했다.
현재는 임상시험 단계 구분 없이 임상시험계획(IND) 접수 후 30일 내 승인하고 있다. 보완사항 등에 대한 검토 후 최종 승인서를 발급하는 방식이다. 반면 호주는 신고제이며 미국, 중국은 심사기간 내 별도 의견이 없을 시 임상시험을 진행하는 승인 간주 형태다. 국내에서도 임상시험 조기 진입을 요구하는 목소리가 커지면서 위험도가 낮은 임상시험부터 차등승인제를 도입하기로 한 것이다. 임상시험 국제 경쟁력을 높이고 국내 환자의 신약 접근성을 지원하기 위해서다.
임상시험 접수 후 5일 이내에 자료를 검토해 알려주는 '예비검토제'도 9월부터 실시하기로 했다. 국내에 치료제가 없는 희귀·난치질환자를 위한 긴급 승인 절차도 마련한다. 임상시험 의약품의 치료목적 사용승인 기간이 현재 7일 이내에서 긴급한 경우 신청 당일 처리되는 식으로 바뀐다.
식약처는 또 임상시험 과정에서 발생하는 의약품의 모든 안전성 정보를 정기적으로 보고하도록 했다. 지금까지는 중대하고 예측하지 못한 부작용 등 주요 안전성 정보만 보고하도록 돼 있다. 임상시험에 참여하는 환자의 안전과 권리 보호를 위해 의료기관과 별도로 공공적 성격의 '중앙임상시험심사위원회'도 운영하고, 심사의 일관성과 효율성 관리를 위한 '임상시험 심사 태스크포스(TF)'도 구성할 계획이다.
식약처는 "임상시험 장기화와 비용 증가가 신약개발 비용 증가의 주원인"이라면서 "임상시험 발전 5개년 종합계획을 통해 신약 개발 강국으로 도약할 것으로 기대한다"고 밝혔다.
조현의 기자 honey@asiae.co.kr
꼭 봐야할 주요뉴스
 "180만원 받으며 225시간 일하지만 계속 일하고파"...
마스크영역
"180만원 받으며 225시간 일하지만 계속 일하고파"...
마스크영역
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>



















![[블룸버그 칼럼]中전기차 무역전쟁, 업계 자멸](https://cwcontent.asiae.co.kr/asiaresize/269/2024041611192825746A.jpg)
![[시시비비] 뉴스 추천 알고리즘의 덫을 피하려면](https://cwcontent.asiae.co.kr/asiaresize/269/2024041611182210159A.jpg)
![[기자수첩]수소 상용화, 中처럼 파괴적 혁신을](https://cwcontent.asiae.co.kr/asiaresize/269/2024041611351983544A.jpg)






![[포토] 세종대왕동상 봄맞이 세척](https://cwcontent.asiae.co.kr/asiaresize/113/2024041610251540828_1713230715.jpg)
![[이미지 다이어리] 짧아진 봄, 꽃놀이 대신 물놀이](https://cwcontent.asiae.co.kr/asiaresize/276/2024041414024738504_1713070967.jpg)
![[포토] 만개한 여의도 윤중로 벚꽃](https://cwcontent.asiae.co.kr/asiaresize/276/2024040809454032284_1712537140.jpg)


![[포토] 3세대 신형 파나메라 국내 공식 출시](https://cwcontent.asiae.co.kr/asiaresize/276/2024040209062225653_1712016383.jpg)
![[뉴스속 용어]전환점에 선 중동의 '그림자 전쟁'](https://cwcontent.asiae.co.kr/asiaresize/113/2024041508192938792_1713136770.jpg)
![[뉴스속 용어]조국혁신당 '사회권' 공약](https://cwcontent.asiae.co.kr/asiaresize/276/2024040408481828594_1712188098.jpg)
![[뉴스속 용어]AI 주도권 꿰찼다, ‘팹4’](https://cwcontent.asiae.co.kr/asiaresize/276/2024040215500326460_1712040603.jpg)
 가장 많이 읽힌 뉴스를 제공합니다. 집계 기준에 따라 최대 3일 전 기사까지 제공될 수 있습니다.
가장 많이 읽힌 뉴스를 제공합니다. 집계 기준에 따라 최대 3일 전 기사까지 제공될 수 있습니다.









