[아시아경제 고형광 기자]
셀트리온
셀트리온
068270
|
코스피
증권정보
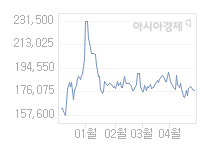 현재가
177,400
전일대비
2,100
등락률
-1.17%
거래량
301,756
전일가
179,500
2024.04.25 15:30 장중(20분지연)
관련기사
'오픈 이노베이션' 속도내는 셀트리온코스피, 외국인·기관 양매도에 2650선 등락 중셀트리온, 램시마SC 필두로 유럽 공략 박차
close
현재가
177,400
전일대비
2,100
등락률
-1.17%
거래량
301,756
전일가
179,500
2024.04.25 15:30 장중(20분지연)
관련기사
'오픈 이노베이션' 속도내는 셀트리온코스피, 외국인·기관 양매도에 2650선 등락 중셀트리온, 램시마SC 필두로 유럽 공략 박차
close
이 개발한 바이오시밀러(바이오의약품 복제약) '허쥬마'가 미국 시장 판매에 한발짝 다가섰다.
셀트리온은 지난 28일(미국 현지 시간) 미국 식품의약국(FDA)에 제출한 유방암 치료용 항암 항체 바이오시밀러 허쥬마(성분명, 트라스투주맙)에 대한 바이오의약품 품목허가신청(BLA)이 받아들여졌다고 31일 밝혔다. 지난 5월 허쥬마의 BLA를 제출한 지 2개월여 만이다.
셀트리온은 미국에서 판매 중인 램시마에 이어 후속 항암 항체 바이오시밀러인 '트룩시마'와 '허쥬마'까지 FDA에 판매 허가를 신청하면서 퍼스트무버 항체 바이오시밀러 제품군 모두 미국 시장 진입을 앞두게 됐다.
허쥬마는 유방암과 위암 등의 치료에 쓰이는 항암 항체 바이오시밀러다. 오리지널의약품은 다국적제약사 제넨텍이 개발한 '허셉틴'이다. 허셉틴은 연간 7조9000억원의 매출을 올리는 세계적 블록버스터 의약품이다. 지난해 미국내 매출만 3조4800억원에 달했다.
셀트리온은 2014년 1월 한국 식품의약품안전처로부터 전이성 유방암과 조기 유방암, 그리고 전이성 위암 치료 용도로 허쥬마의 허가를 받았고 올 하반기 국내 시판을 준비 중이다. 지난해 10월엔 유럽의약품청(EMA)에, 지난 4월엔 일본 후생노동성에 각각 판매 허가를 신청한 상태다.
기우성 셀트리온 대표이사는 "허쥬마는 풍부한 임상 데이터를 바탕으로 오리지널 제품과 동등한 안전성과 유효성을 입증했고 저명 학술지인 란셋(Lancet)에도 임상 논문이 게재되는 등 경쟁제품 대비 우월한 임상 결과를 확보했다"며 "허가 승인과 출시까지 기간이 남아 있으나 항암제 분야에서도 업계 선도적으로 미국 내 더 많은 환자들에게 치료 혜택을 제공할 수 있도록 최선을 다하겠다"고 말했다.
고형광 기자 kohk0101@asiae.co.kr
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>













![잠시 쉴 틈도 없는 치매 보호자…'하루 1만원' 내고 휴가 보내줄도 알아야[노인 1000만 시대]⑥](https://cwcontent.asiae.co.kr/asiaresize/269/2024041515134639824_1713161625.jpg)







![[초동시각]제 대답은 '아니오' 입니다](https://cwcontent.asiae.co.kr/asiaresize/269/2024042511111216547A.jpg)
![[시시비비]경영권 지킨 디즈니와 'PC주의' 논란](https://cwcontent.asiae.co.kr/asiaresize/269/2024042513390549754A.jpg)
![[특별기고]세계 경제 불확실성이 주는 투자 기회](https://cwcontent.asiae.co.kr/asiaresize/269/2024042513464837251A.jpg)






![[포토] 정교한 3D 프린팅의 세계](https://cwcontent.asiae.co.kr/asiaresize/113/2024042410323050257_1713922350.jpg)
![[포토] '그날의 기억'](https://cwcontent.asiae.co.kr/asiaresize/276/2024041909431345253_1713487393.jpg)
![[이미지 다이어리] 그곳에 목련이 필 줄 알았다.](https://cwcontent.asiae.co.kr/asiaresize/276/2024041808095443462_1713395394.jpg)



![[뉴스속 인물]하이브에 반기 든 '뉴진스의 엄마' 민희진](https://cwcontent.asiae.co.kr/asiaresize/113/2024042510502452065_1714009823.png)
![[뉴스속 용어]뉴스페이스 신호탄, '초소형 군집위성'](https://cwcontent.asiae.co.kr/asiaresize/276/2024042415131250718_1713939192.jpg)
![[뉴스속 용어]日 정치인 '야스쿠니신사' 집단 참배…한·중 항의](https://cwcontent.asiae.co.kr/asiaresize/276/2023042111281396915_1682044092.jpg)
 가장 많이 읽힌 뉴스를 제공합니다. 집계 기준에 따라 최대 3일 전 기사까지 제공될 수 있습니다.
가장 많이 읽힌 뉴스를 제공합니다. 집계 기준에 따라 최대 3일 전 기사까지 제공될 수 있습니다.











