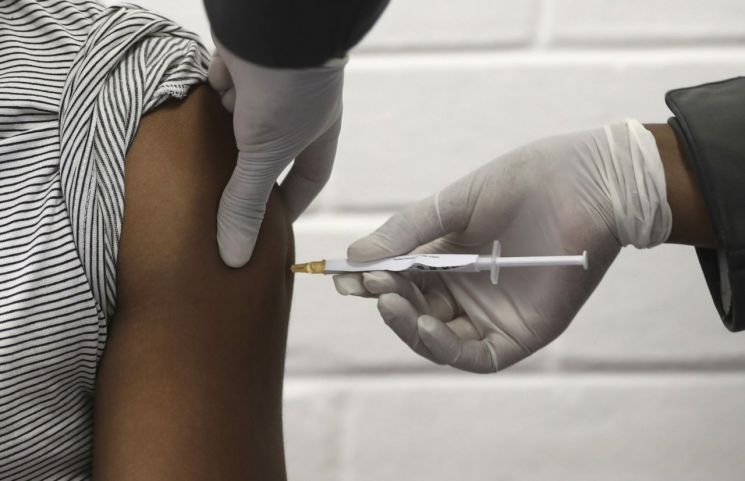
[아시아경제 우수연 기자]영국 정부가 영국 제약사 아스트라제네카와 옥스퍼드대가 공동 개발중인 신종 코로나바이러스감염증(코로나19) 백신에 대해 승인 절차에 돌입했다.
27일(현지시간) 주요 외신에 따르면 영국 보건부는 의약품건강관리제품규제청(MHRA)에 옥스퍼드대-아스트라제네카 백신의 적합성 평가를 요청했다. 영국에서 백신 허가를 위해서는 가장 먼저 정부가 MHRA에 공식 평가를 요청해야한다.
MHRA는 이미 관련 자료를 넘겨 받아 단계적 검토 절차에 돌입했다. 영국 정부는 만약 백신이 최종 승인 될 경우 연내 400만개, 내년 3월말까지 4000만개의 백신을 확보할 수 있을 것으로 전망했다. 지난 20일 영국 정부는 화이자-바이오엔테크 백신에 대한 적합성 평가도 MHRA에 요청한 바 있다.
앞서 옥스퍼드대와 아스트라제네카는 개발중인 백신의 3상 임상시험 초기 데이터 분석 결과 평균 면역 효과가 70%로 나타났다고 발표했다.
하지만 백신 1회분의 절반을 우선 투약하고 한달 후 1회분을 온전히 투약한 참가자들은 90%, 두 차례 모두 1회분 전체 용량을 투약한 이들의 예방효과는 62%였다. 연구진은 투약량에 따른 면역 효과 차이의 원인을 아직까지 밝혀내지 못했다.
이 같은 백신 신뢰성에 대한 의문이 제기되자 파스칼 소리오 아스트라제네카 CEO는 저용량 투약 방식에 대한 추가 글로벌 임상 시험을 진행하겠다고 밝혔다.
우수연 기자 yesim@asiae.co.kr
꼭 봐야할 주요뉴스
 성인 절반 "어버이날 '빨간날'로 해 주세요"…60대...
마스크영역
성인 절반 "어버이날 '빨간날'로 해 주세요"…60대...
마스크영역
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>












![잠시 쉴 틈도 없는 치매 보호자…'하루 1만원' 내고 휴가 보내줄도 알아야[노인 1000만 시대]⑥](https://cwcontent.asiae.co.kr/asiaresize/269/2024041515134639824_1713161625.jpg)







![[초동시각]제 대답은 '아니오' 입니다](https://cwcontent.asiae.co.kr/asiaresize/269/2024042511111216547A.jpg)
![[시시비비]경영권 지킨 디즈니와 'PC주의' 논란](https://cwcontent.asiae.co.kr/asiaresize/269/2024042513390549754A.jpg)
![[특별기고]세계 경제 불확실성이 주는 투자 기회](https://cwcontent.asiae.co.kr/asiaresize/269/2024042513464837251A.jpg)






![[포토] 정교한 3D 프린팅의 세계](https://cwcontent.asiae.co.kr/asiaresize/113/2024042410323050257_1713922350.jpg)
![[포토] '그날의 기억'](https://cwcontent.asiae.co.kr/asiaresize/276/2024041909431345253_1713487393.jpg)
![[이미지 다이어리] 그곳에 목련이 필 줄 알았다.](https://cwcontent.asiae.co.kr/asiaresize/276/2024041808095443462_1713395394.jpg)



![[뉴스속 인물]하이브에 반기 든 '뉴진스의 엄마' 민희진](https://cwcontent.asiae.co.kr/asiaresize/113/2024042510502452065_1714009823.png)
![[뉴스속 용어]뉴스페이스 신호탄, '초소형 군집위성'](https://cwcontent.asiae.co.kr/asiaresize/276/2024042415131250718_1713939192.jpg)
![[뉴스속 용어]日 정치인 '야스쿠니신사' 집단 참배…한·중 항의](https://cwcontent.asiae.co.kr/asiaresize/276/2023042111281396915_1682044092.jpg)
 가장 많이 읽힌 뉴스를 제공합니다. 집계 기준에 따라 최대 3일 전 기사까지 제공될 수 있습니다.
가장 많이 읽힌 뉴스를 제공합니다. 집계 기준에 따라 최대 3일 전 기사까지 제공될 수 있습니다.










